题目内容
【题目】X溶液中含有下表所示离子中的某5种,且其离子浓度均为![]() (不考虑水的电离和离子水解)。向X溶液中加入足量稀盐酸,有气体生成,反应前后阴离子种类不变。下列叙述错误的是( )
(不考虑水的电离和离子水解)。向X溶液中加入足量稀盐酸,有气体生成,反应前后阴离子种类不变。下列叙述错误的是( )
阳离子 |
|
阴离子 |
|
A.原溶液中一定含有![]()
B.X溶液中不可能含有![]() 和
和![]()
C.X溶液中含有3种阳离子、2种阴离子
D.生成气体的离子反应方程式为![]()
【答案】C
【解析】
各种离子的物质的量浓度均为0.1mol/L,向溶液X中加入足量的盐酸,有气体生成,且反应溶液中阴离子的种类没有变化,产生气体不可能是二氧化碳,则不含OH-、HCO3-和CO32-;根据表中的离子,可推知是Fe2+、NO3-在酸性环境下生成的一氧化氮,加入盐酸,生成气体的离子反应方程式为![]() ,NO3-反应后有剩余,故溶液中阴离子种类不变,所以原来溶液中含有Cl﹣。由于总共含有5种离子,根据电荷守恒及离子共存的条件可以判断还含有SO42﹣和Mg2+,所以原溶液中含有的五种离子为:Cl﹣、NO3-、SO42﹣、Fe2+、Mg2+。
,NO3-反应后有剩余,故溶液中阴离子种类不变,所以原来溶液中含有Cl﹣。由于总共含有5种离子,根据电荷守恒及离子共存的条件可以判断还含有SO42﹣和Mg2+,所以原溶液中含有的五种离子为:Cl﹣、NO3-、SO42﹣、Fe2+、Mg2+。
A.根据分析可知,原溶液中一定含有Mg2+,A正确;
B.加入足量盐酸后阴离子种类不变, HCO3-和CO32与-H+反应后就不h存在b了 ,B正确;
C.根据分析可知,原溶液中含有的五种离子为Cl﹣、NO3﹣、SO42﹣、Fe2+、Mg2+,共有2种阳离子、3种阴离子,C错误;
D. Fe2+ 与NO3﹣、H+反应时Fe2+被氧化为三价铁,硝酸根被还原为NO,生成气体的离子反应方程式为![]() ,D正确。
,D正确。
答案选C。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案【题目】某同学在实验室做铜与浓硫酸反应的实验。
(1)写出反应的化学方程式_____。
停止加热,将试管中的混合物冷却后倒入装有冷水的烧杯中,搅拌、静置,观察到烧杯底部有黑色物质。于是他对黑色物质进行了探究。
(2)该同学假设黑色物质CuO。检验过程如下:
(查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+)该同学的实验操作:
①将CuO放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,产生红褐色沉淀。
②将黑色物质放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀。实验①的目的是__________,由该检验过程所得结论是________。
(3)再次假设,黑色物质是铜的硫化物。实验如下:
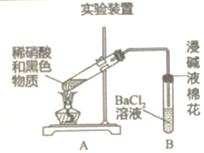
实验装置
| 现象 1.A试管中黑色沉淀逐渐溶解 2.A试管内上方出现浅红棕色气体 3.B试管中出现…… |
①现象2说明黑色物质具有________性。
② A试管内上方出现浅红棕色气体的化学方程式是__________。
③能确认黑色沉淀中含有S元素的现象_________。
(4)以上实验说明,黑色物质中存在铜的硫化物。进一步实验后证明黑色物质是 CuS与Cu2S的混合物。已知1molCu2S与稀硝酸反应转移8mole-,写出试管A中Cu2S 溶解的化学方程式____________。