题目内容
X、Y、Z三种物质有如图所示转化关系:
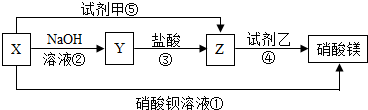
(1)根据上述转化关系,写出下列物质的化学式:
X 、Y 、Z ;试剂甲 ,试剂乙 .
(2)写出上述各步反应①~⑤的离子方程式:
① ;② ;③ ;
④ ;⑤ .

(1)根据上述转化关系,写出下列物质的化学式:
X
(2)写出上述各步反应①~⑤的离子方程式:
①
④
考点:无机物的推断
专题:推断题
分析:根据X和硝酸钡反应会生成硝酸镁,所以依据复分解反应的原理可知,X中有镁离子,还的会与钡离子生成沉淀,可能含有硫酸根离子或碳酸根离子,碳酸镁是沉淀,所以X就是硫酸镁,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,Y与盐酸反应得到Z,所以Y是氢氧化镁,氢氧化镁和盐酸反应生成氯化镁和水,所以Z是氯化镁,氯化镁和乙反应会生成硝酸镁,所以乙是硝酸银,硫酸镁和甲反应生成氯化镁,所以甲就是氯化钡,据此解答.
解答:
解:(1)X和硝酸钡反应会生成硝酸镁,所以依据复分解反应的原理可知,X中有镁离子,还会与钡离子生成沉淀,可能含有硫酸根离子或碳酸根离子,碳酸镁是沉淀,所以X就是硫酸镁,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,Y与盐酸反应得到Z,所以Y是氢氧化镁,氢氧化镁和盐酸反应生成氯化镁和水,所以Z是氯化镁,氯化镁和乙反应会生成硝酸镁,所以乙是硝酸银,硫酸镁和甲反应生成氯化镁,所以甲就是氯化钡,经过验证,各物质都满足转换关系,
故答案为:X:MgSO4,Y:Mg(OH)2,Z:MgCl2 ,BaCl2,AgNO3;
(2)①硫酸根离子和钡离子生成硫酸钡沉淀,故答案为:SO42-+Ba2+=BaSO4↓;
②镁离子和氢氧根离子生成氢氧化镁沉淀,故答案为:Mg2++2OH-=Mg(OH)2↓;
③氢氧化镁和氢离子反应生成镁离子和水,故答案为:Mg(OH)2+2H+=Mg2++2H2O;
④银离子和氯离子反应生成氯化银沉淀,故答案为:Ag++Cl-=AgCl↓;
⑤硫酸根离子和钡离子反应生成硫酸钡沉淀,故答案为:SO42-+Ba2+=BaSO4↓.
故答案为:X:MgSO4,Y:Mg(OH)2,Z:MgCl2 ,BaCl2,AgNO3;
(2)①硫酸根离子和钡离子生成硫酸钡沉淀,故答案为:SO42-+Ba2+=BaSO4↓;
②镁离子和氢氧根离子生成氢氧化镁沉淀,故答案为:Mg2++2OH-=Mg(OH)2↓;
③氢氧化镁和氢离子反应生成镁离子和水,故答案为:Mg(OH)2+2H+=Mg2++2H2O;
④银离子和氯离子反应生成氯化银沉淀,故答案为:Ag++Cl-=AgCl↓;
⑤硫酸根离子和钡离子反应生成硫酸钡沉淀,故答案为:SO42-+Ba2+=BaSO4↓.
点评:本题考查无机物推断,根据复分解反应确定X是关键,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可,难点不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、相同物质的量浓度时,溶液中c(NH4+)由大到小的顺序:NH4Al(SO4)2>NH4Cl>CH3COONH4>NH3?H2O |
| B、为了确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C、0.2mol?L-1的CH3COONa溶液与0.1mol?L-1的HCl等体积混合呈酸性:c(Na+)>c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) |
| D、相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1mol/L盐酸、③0.1mol/L氯化镁溶液、④0.1mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ |
下列反应中硝酸既表现出了强氧化性又表现了酸性的是( )
| A、氧化铁与硝酸反应 |
| B、氢氧化铝与硝酸反应 |
| C、木炭粉与浓硝酸反应 |
| D、铜与硝酸反应 |


 根据氧化还原反应:Zn(s)+2Ag+(aq)═Zn2+(aq)+2Ag(s),试设计一个简单的原电池.
根据氧化还原反应:Zn(s)+2Ag+(aq)═Zn2+(aq)+2Ag(s),试设计一个简单的原电池.