题目内容
【题目】在一定温度下,将SO2与足量O2置于密闭容器中发生反应。SO2与SO3的物质的量浓度随时间的变化如图所示,请回答下列问题。
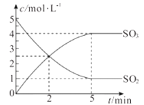
(1)0~2min以SO2表示的化学反应速率为_____mol·L-1min-1。
(2)5min后c(SO2)与c(SO3)不再随时间改变的原因是_________。
(3)由图像可知SO2与O2的反应是可逆反应,理由是_________。
【答案】1.25 正、逆反应速率相等,反应达到了平衡状态 SO2、SO3的浓度不再改变,且均不为0
【解析】
SO2与O2反应生成SO3属于可逆反应,2SO2+O2![]() 2SO3,可逆反应不能完全进行到底,从化学平衡状态的定义;化学反应速率的计算,需要利用其数学表达式进行,据此分析;
2SO3,可逆反应不能完全进行到底,从化学平衡状态的定义;化学反应速率的计算,需要利用其数学表达式进行,据此分析;
(1)化学反应速率是单位时间内反应物浓度或生成物浓度的变化,0~2min,用SO2表示的反应速率是![]() =1.25mol/(L·min);
=1.25mol/(L·min);
(2)5min后,c(SO2)与c(SO3)不再随时间改变是由于正、逆反应速率相等,反应达到了平衡状态;
(3)由图像可知,5min后SO2、SO3的浓度不再改变,且均不为0,说明5min后正逆反应速率相等,反应达到平衡状态,该反应为可逆反应。

【题目】某小组研究第3周期元素性质的递变规律,设计了如下实验,并记录了实验现象:
实验步骤 | 实验现象 |
①将一小块钠放入滴有酚酞的冷水中 | A.有气体产生,溶液变成浅红色 |
②将用砂纸打磨过的镁条放入沸水中,再向其中滴加少量酚酞溶液 | B.浮在水面上,熔成小球,做不定向运动,随后消失,溶液变为红色 |
③将镁条放入稀盐酸中 | C.反应较快,产生无色气体 |
④将铝条放入稀盐酸中 | D.反应剧烈,迅速产生大量无色气体 |
(1)补齐实验步骤与实验现象之间的连线___________。

(2)由上述实验可知Na、Mg、Al三种元素原子失电子能力(金属性)依次_______(填“增强”或“减弱”)。从原子结构的角度解释原因____________。
(3)比较第3周期中硫与氯两种元素原子得电子能力(非金属性)的相对强弱。
①甲同学设计的下列方法可行的是_______。
A.比较气态氢化物的稳定性 B.比较盐酸与硫酸的酸性 C.比较单质与酸反应置换出氢气的难易程度
②乙同学设计将氯气通入硫化钠溶液中,观察是否有淡黄色沉淀生成。这一实验的设计思路是通过比较________,推知元素原子得电子能力的相对强弱。
(4)利用元素周期律可预测陌生元素及物质的性质,已知Rb与Na处于同一主族,下列说法正确的是_____。
A.失电子能力:Rb>Na B.碱性:NaOH>RbOH C.Rb比Na更容易与氧气发生反应 D.Rb不易与水反应放出H2