题目内容
【题目】如图所示,若电解5min时铜电极质量增加2.16g,B池的两极都有气体产生。试回答:

(1)电源电极X名称为_________(填“正极”或“负极”)
(2)烧杯中溶液的 pH变化:(填“增大”、“减小”或“不变”)B池________________,C池________________。
(3)写出A池中所发生的电解反应方程式:_________________
【答案】负极 减小 不变 2KCl+2H2O![]() 2KOH+H2↑ + Cl2↑
2KOH+H2↑ + Cl2↑
【解析】
根据题中装置图可知,本题考查原电池知识,运用活泼金属电极做负极,较不活泼金属电极做正极分析。
(1)若电解5min时铜电极质量增加2.16g,说明铜电极为阴极,则银电极为阳极,则X为负极,Y为正极,
故答案为:负极;
(2)B中电解硫酸铜溶液生成硫酸,溶液中氢离子浓度增大,pH减小,C中阴极反应为Ag++e-=Ag,阳极反应为Ag-e-=Ag+,溶液浓度不变,则pH不变,
故答案为:减小;不变;
(3)A池中发生反应为电解氯化钾溶液的反应,电解反应方程式为:2KCl+2H2O![]() 2KOH+H2↑ + Cl2↑,
2KOH+H2↑ + Cl2↑,
故答案为:2KCl+2H2O![]() 2KOH+H2↑ + Cl2↑。
2KOH+H2↑ + Cl2↑。

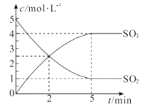
【题目】一定温度下,向2.0L恒容密闭容器中充入2molSO2和1molO2,发生反应为:2SO2(g)+O2(g) ![]() 2SO3(g)。经过一段时间后达到平衡,反应过程中测定的部分数据见下表:下列说法正确的是( )
2SO3(g)。经过一段时间后达到平衡,反应过程中测定的部分数据见下表:下列说法正确的是( )
t/s | 0 | 2 | 4 | 6 | 8 |
n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
A.反应在前2 s的平均速率υ(O2)=0.4 mol·L1·s1
B.保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C.相同温度下,起始时向容器中充入4 mol SO3,达平衡时,SO3的转化率大于10%
D.保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2) 增大