题目内容
9.下列各组中的三种微粒,所含质子数与电子数都相等的是( )| A. | Na+、Mg2+、Al3+ | B. | HCl、H2S、Ar | C. | H2O、OH-、Na+ | D. | NH4+、Na+、F- |
分析 A、Na+、Mg2+、Al3+的质子数分别为:11、12、13;
B、HCl、H2S、Ar的质子数分别为:18、18、18,电子数分别为18,18、18;
C、H2O、OH-、Na+的质子数分别为:10、9、11;
D、NH4+、Na+、F-的质子数分别为:11、11、9.
解答 解:A、Na+、Mg2+、Al3+的质子数分别为:11、12、13,电子数分别为10,10、10,故A错误;
B、HCl、H2S、Ar的质子数分别为:18、18、18,电子数分别为18,18、18,故B正确;
C、H2O、OH-、Na+的质子数分别为:10、9、11、电子数分别为10,10、10,故C错误;
D、NH4+、Na+、F-的质子数分别为:11、11、9、电子数分别为10,10、10,故D错误;
故选B.
点评 掌握质子数的计算方法是分子或离子中各种元素的质子数与其对应的原子个数的乘积,再加在一起,电子数计算方法是先计算出质子数,再看整体如果是失去电子,失去了几个电子就减去几,得了几个电子就加上几.

练习册系列答案
相关题目
10.现有Wg某不饱和链烃R(R分子中只含单键和双键),R能与VL(标准状况)氢气恰好完全反应,生成烷烃.若R的相对分子质量为M,阿伏加德罗常数为NA,则lmol R中含有双键数目为( )
| A. | $\frac{WV{N}_{A}}{22.4M}$ | B. | $\frac{MV{N}_{A}}{22.4W}$ | C. | $\frac{WV}{22.4M}$ | D. | $\frac{MV}{22.4W}$ |
17.下表标出的是元素周期表的一部分元素,回答下列问题:
(1)表中用字母标出的14种元素中,化学性质最不活泼的是Ar(用元素符号表示,下同),金属性最强的是K,非金属性最强的是F常温下单质为液态的非金属元素是Br,属于过度元素的是M(该空用字母表示).
(2)B,F,C的气态氢化物中以PH3最不稳定(填化学式).
(3)除稀有气体外第三周期中原子半径最小的是Cl(填元素符号)
(4)写出I、H号元素最高价氧化物的对应水化物的化学式:Mg(OH)2和Al(OH)3.强弱顺序是Mg(OH)2>Al(OH)3.
| 1 | ||||||||||||||||||
| 2 | D | B | A | |||||||||||||||
| 3 | J | I | H | C | G | F | E | |||||||||||
| 4 | L | K | M | N | ||||||||||||||
(2)B,F,C的气态氢化物中以PH3最不稳定(填化学式).
(3)除稀有气体外第三周期中原子半径最小的是Cl(填元素符号)
(4)写出I、H号元素最高价氧化物的对应水化物的化学式:Mg(OH)2和Al(OH)3.强弱顺序是Mg(OH)2>Al(OH)3.
4.化学与人类生活、工农业生产、科学技术等息息相关,下列说法正确的是( )
| A. | 在涂料中尽量用液态有机物代替水作溶剂以减少环境污染 | |
| B. | 世博会很多场馆的外壳使用非晶硅薄膜,以充分利用太阳能,体现低碳经济 | |
| C. | 石油分馏可获得乙烯、丙烯和丁二烯 | |
| D. | 绿色化学的核心是应用化学原理对环境污染进行治理 |
14.下列说法中正确的是( )
| A. | CO2、NH3、BF3中,所有原子都满足最外层8电子的稳定结构 | |
| B. | 在元素周期表中金属和非金属交界处可以找到半导体材料 | |
| C. | 由非金属元素组成的化合物一定是共价化合物 | |
| D. | 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键 |
1.最近,日本在一公园内检测到放射性物质包括碘131和铯137,引起社会恐慌.有关资料显示其中,碘131一旦被人体吸入,可能会引发甲状腺疾病,铯137则会造成人体造血系统和神经系统损伤.请问这两个原子53131I和55137Cs的核内中子数分别为( )
| A. | 53和55 | B. | 131和137 | C. | 78和82 | D. | 76和79 |
18.常温时,向pH=2的硫酸中加入等体积的下列溶液后,滴入甲基橙试液,出现红色,该溶液可能是( )
| A. | pH=12 的Ba(OH)2 | B. | pH=12的氨水 | C. | 0.005mol/L NaOH | D. | 0.05mol/L BaCl2 |
19.下列物质的变化,不能通过一步化学反应完成的是( )
| A. | CO2→H2CO3 | B. | SiO2→Na2SiO3 | C. | SiO2→H2SiO3 | D. | Na2O2→Na2CO3 |
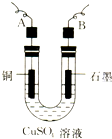 某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器如下图所示,回答下列问题:
某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器如下图所示,回答下列问题: