题目内容
1.下列关于元素周期表的说法中,错误的是( )| A. | 元素原子的最外层电子数等于其所在族的序数 | |
| B. | 元素原子的电子层等于其所在周期的序数 | |
| C. | 同一主族元素的原子最外层电子数相同,化学性质相似 | |
| D. | 元素周期表是元素周期律的具体表现形式 |
分析 A、主族元素原子的最外层电子数=族序数;
B、元素原子的周期数=电子层数;
C、同一主族的元素原子,最外层电子数相同,化学性质具有相似性;
D、元素周期律是核外电子周期性变化的必然结果.
解答 解:A、主族元素原子的最外层电子数=族序数,如Na最外层有1个电子,则族序数为1,即主族元素原子的最外层电子数等于其所在族的族序数,故A错误;
B、元素原子的周期数=电子层数,所以元素原子的电子层数等于其所在周期的周期序数,故B正确;
C、同一主族的元素原子,最外层电子数相同,最外层电子数决定其化学性质,但随着原子半径的增大,原子核对核外电子吸引能力逐渐减弱,所以其化学性质具有相似性也有递变性,故C正确;
D、元素周期律是核外电子周期性变化的必然结果,则元素周期表是元素周期律的具体表现形式,故D正确;
故选A.
点评 本题考查元素周期律,题目难度不大,熟悉元素在周期表中的位置及元素的性质即可解答,注重元素位置与性质的考查.

练习册系列答案
相关题目
12.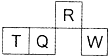 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R<Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | T的氧化物既能与强酸反应又能与强碱反应 |
9.下列说法中正确的是( )
| A. | 次外层电子数是2或8的原子一定不是副族元素 | |
| B. | 稀有气体的原子的电子排布最外层都是以P6结束 | |
| C. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 | |
| D. | 核外电子排布相同的微粒,一定具有相同的化学性质 |
16.燃烧某有机物只生成二氧化碳8.8g和水2.7g,下列说法中,正确的是( )
| A. | 该有机物的最简式为C2H3 | |
| B. | 该有机物分子中肯定不含有碳碳叁键 | |
| C. | 该有机物不可能含有氧元素 | |
| D. | 该有机物不可能是丁烷 |
6.某同学做同族元素性质相似性、递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助同学整理并完成实验报告:
(1)实验目的:探究同主族元素性质的相似性与递变性
(2)实验用品:
①试剂:金属钠、金属钾、新制氯水、溴水、0.1mol/LNaBr溶液、0.1mol/LNaI溶液、CCl4等.
②仪器:胶头滴管、试管、烧杯、镊子、小刀、玻璃片等.
(3)实验内容(填写与实验方案对应的实验现象的标号及化学方程式和离子方程式)
(4)实验结论:同主族元素性质相似,自上而下元素金属性增强,非金属性减弱.
| 实验方案 | 实验现象 |
| ①将氯水滴加到溴化钠溶液中,振荡后加入适量CCl4溶液,振荡,静置 | A.浮在水面,熔成小球,不定向移动,随之消失 |
| ②将一小块金属钠放入冷水中 | B.分层,上层无色,下层紫红色 |
| ③将溴水滴加到NaI溶液中,振荡后加入适量CCl4溶液,振荡,静置 | C.浮在水面,熔成小球,不定向移动,并伴有轻微的爆炸声,很快消失 |
| ④将一小块金属钾放入冷水中 | D.分层,上层无色,下层橙红色 |
(1)实验目的:探究同主族元素性质的相似性与递变性
(2)实验用品:
①试剂:金属钠、金属钾、新制氯水、溴水、0.1mol/LNaBr溶液、0.1mol/LNaI溶液、CCl4等.
②仪器:胶头滴管、试管、烧杯、镊子、小刀、玻璃片等.
(3)实验内容(填写与实验方案对应的实验现象的标号及化学方程式和离子方程式)
| 实验方案 | 实验现象 | 化学方程式 | 离子方程式 |
| ① | |||
| ② | |||
| ③ | |||
| ④ |
13.饱和氯水久置后,溶液中的各种粒子:①Cl2 ②H+ ③Cl- ④HClO 减少的是( )
| A. | ①②④ | B. | ①②③ | C. | ①④ | D. | ②④ |
10.下列电离方程式中,正确的是( )
| A. | Na2SO4=2Na++SO4-2 | B. | H2CO3=2H++CO32- | ||
| C. | Al2 (SO4)3=2Al3++3 SO42- | D. | Ca(NO3)2=Ca2++2(NO3)2- |