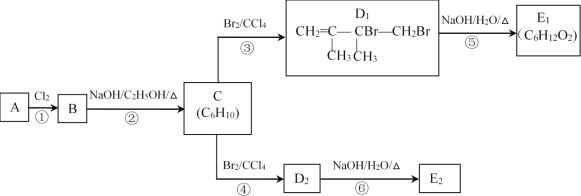
题目内容
【题目】由含碘废水制取碘酸钾的一种工艺如下:
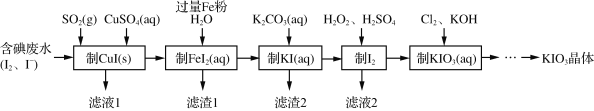
(1)H2O2的结构式为___。“制I2”过程中加入的硫酸不能过多的原因是_____。
(2)制CuI(s)步骤反应的离子方程式为_________。
(3)工艺中五种物质的制备反应中,不涉及氧化还原反应的步骤是“制___”。
(4)“制KI(aq)”时,该温度下水的离子积为Kw=1.0×10-13,Ksp[Fe(OH)2]=9.0×10-15。为避免0.9 mol·L-1 FeI2溶液中Fe2+水解生成胶状物吸附I-,起始加入K2CO3必须保持溶液的pH不大于________。
(5)“制KIO3溶液”反应的离子方程式为______。
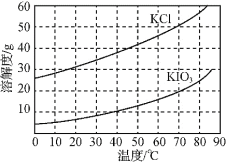
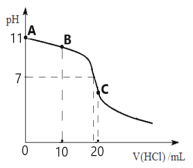
(6)KCl、KIO3的溶解度曲线如图所示。流程中由“KIO3(aq)”得到KIO3晶体的操作步骤为____。
【答案】H—O—O—H 会导致在“制KIO3(aq)”步骤中加入的KOH量过多,浪费试剂 2SO2+I2+2Cu2++4H2O=2CuI↓+2SO42-+8H+ KI(aq) 6.0 5Cl2+I2+12OH-=2IO3-+10Cl-+6H2O 蒸发浓缩,冷却结晶(过滤) (2分,“过滤”答不答都给分)
【解析】
根据流程:含碘废水中加入二氧化硫和硫酸铜发生发应:2SO2+I2+2Cu2++4H2O═2CuI↓+SO42-+8H+制备CuI(s),过滤,滤液1含硫酸,向滤渣中加入铁粉、水,发生反应:2CuI+Fe=2Cu+FeI2,制得FeI2(aq),过滤得到的滤渣1为Fe和Cu,滤液中加入碳酸钾发生反应:K2CO3+FeI2=FeCO3↓+2KI,滤渣2为FeCO3,酸性条件下,KI、过氧化氢发生氧化还原反应:2I-+2H++H2O2=H2O+I2生成碘单质,滤液2含有硫酸钾,碘单质、氯气、KOH发生反应5Cl2+I2+12OH-═2IO3-+10Cl-+6H2O,得到含有KIO3的溶液,经过蒸发浓缩,降温结晶得到KIO3晶体。
(1) H2O2的电子式为:![]() ,结构式H—O—O—H;答案为H—O—O—H;硫酸后面要加KOH,故答案为:会导致在“制KIO3(aq)”步骤中加入的KOH量过多,浪费试剂;
,结构式H—O—O—H;答案为H—O—O—H;硫酸后面要加KOH,故答案为:会导致在“制KIO3(aq)”步骤中加入的KOH量过多,浪费试剂;
(2) 通入SO2的目的是将I2还原为I,其自身被氧化为为SO42,离子反应为:2SO2+I2+2Cu2++4H2O=2CuI↓+2SO42-+8H+,故答案为:2SO2+I2+2Cu2++4H2O=2CuI↓+2SO42-+8H+;
(3) 根据分析,KI(aq)的生成无化合价升降变化,为非氧化还原反应,故答案为:KI(aq);
(4) 已知:Ksp[Fe(OH)2]=9.0×1015,现测得c( FeI2)=0.9 molL1,则由公式算的c(OH)=L=107mol/L,此温度下,Kw=1.0×1013,则c(H+)=(1×1013/107)mol/L=106mol/L,故pH=6.0,故答案为:6.0;
(5) 根据分析,“制KIO3溶液”反应的离子方程式为:5Cl2+I2+12OH-=2IO3-+10Cl-+6H2O,故答案为:5Cl2+I2+12OH-=2IO3-+10Cl-+6H2O;
(6)根据KCl、KIO3的溶解度曲线,将“KIO3(aq)”蒸发浓缩,降温结晶得到KIO3晶体,故答案为:蒸发浓缩,降温结晶。

 学业测评一课一测系列答案
学业测评一课一测系列答案【题目】CO、H2是煤的气化产物,在生产生活中用途广泛。
(1)CO还原法处理大气污染物SO2
①2CO(g) + SO2(g) ![]() S(s)+2CO2(g) H = -270 kJ·mol-1,该反应的平衡常数表达式为__。
S(s)+2CO2(g) H = -270 kJ·mol-1,该反应的平衡常数表达式为__。
②在绝热恒容的密闭容器中进行上述反应,下列说法正确的是_____。
a 若混合气体密度保持不变,则已达平衡状态
b 达平衡后若再充人一定量CO2,平衡常数保持不变
c 分离出部分S,正、逆反应速率均保持不变,平衡不移动
d 从反应开始到平衡,容器内气体的压强保持不变
③向2 L恒温恒容密闭容器中通人2 mol CO、1 mol SO2,分别进行a、b、c三组实验。在不同催化剂件下发生反应:2CO(g) + SO2(g) ![]() S(s)+2CO2(g) H = -270 kJ·mol-1,反应体系总压随时间的变化如下表所示,则三组实验温度的大小关系是_____(用a、b、c表示),实验a从反应开始至45s达到平衡,则该过程反应速率v(SO2)__________(结果保留2位有效数字)。
S(s)+2CO2(g) H = -270 kJ·mol-1,反应体系总压随时间的变化如下表所示,则三组实验温度的大小关系是_____(用a、b、c表示),实验a从反应开始至45s达到平衡,则该过程反应速率v(SO2)__________(结果保留2位有效数字)。
| 0s | 40s | 45s | 60s |
a | 175 | 142 | 140 | 140 |
b | 160 | 120 | 120 | 120 |
c | 160 | 130 | 125 | 120 |
(2)利用CO、H2可制备天然气,主要反应为:
CO(g) + 3H2(g) ![]() CH4(g) + H2O(g) H1=-206.2 kJ·mol1;
CH4(g) + H2O(g) H1=-206.2 kJ·mol1;
CO(g) + H2O(g) ![]() CO2(g) + H2(g) H2 = -41.0 kJ·mol-1;
CO2(g) + H2(g) H2 = -41.0 kJ·mol-1;
H2O(l) ═H2O(g) H3 =+44 kJ·mol-1 。
回答下列问题:
①反应CO2(g) + 4H2(g) ![]() CH4(g) + 2H2O(l) 的H4 = ________ kJ·mol-1。某温度下,分别在起始容积相同的恒压容器A、恒容容器B中加人1molCO2和4molH2的混合气体,两容器反应达到平衡后放出或吸收的热量较多的是__( 填“A”或“B")。
CH4(g) + 2H2O(l) 的H4 = ________ kJ·mol-1。某温度下,分别在起始容积相同的恒压容器A、恒容容器B中加人1molCO2和4molH2的混合气体,两容器反应达到平衡后放出或吸收的热量较多的是__( 填“A”或“B")。
②在恒压管道反应器中按n(H2):n(CO) = 3:1通入原料气,在催化剂作用下制备合成天然气,400 ℃ p总为100 kPa时反应体系平衡组成如下表所示:
组分 | CH4 | H2O | H2 | CO2 | CO |
体积分数/% | 45.0 | 42.5 | 10.0 | 1.50 | 1.00 |
则该条件下CO的总转化率α=____。![]()
③制备合成天然气采用在原料气中通入水蒸气来缓解催化剂积碳。
积碳反应为:反应I :CH4(g) ![]() C(s) + 2H2(g) H = +75 kJ·mol-1;
C(s) + 2H2(g) H = +75 kJ·mol-1;
反应Ⅱ:2CO(g) ![]() C(s) + CO2(g) H = -172 kJ·mol-1,
C(s) + CO2(g) H = -172 kJ·mol-1,
平衡体系中水蒸气浓度对积碳量的影响如图所示,下列说法正确的是__。
A 曲线1在700 ~ 800℃积碳量减小的原因可能是反应Ⅱ逆向移动
B 曲线1在550 ~700℃积碳量增大的原因可能是反应I、Ⅱ的速率增大
C 曲线2、3在550 ~800℃积碳量较低的原因是水蒸气稀释作用使积碳反应速率减小
D 水蒸气能吸收反应放出的热量,降低体系温度至550℃以下,有利于减少积碳