题目内容
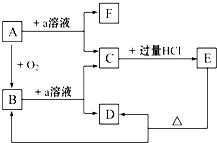 在下列物质的转化关系中,A是一种固体单质,且常作半导体材料,E是一种白色沉淀,F是最轻的气体单质.据此填写:
在下列物质的转化关系中,A是一种固体单质,且常作半导体材料,E是一种白色沉淀,F是最轻的气体单质.据此填写:(1)B的化学式是
(2)B和a溶液反应的离子方程式是
(3)C和过量盐酸反应的离子方程式是
考点:无机物的推断,硅和二氧化硅
专题:推断题,碳族元素
分析:A是一种固体单质,且常作半导体材料,A应为Si,F是最轻的气体单质,应为H2,
a溶液是强碱(如NaOH)溶液或HF溶液,而Si和SiO2与NaOH溶液反应均生成Na2SiO3.Na2SiO3与过量盐酸反应生成NaCl和H2SiO3白色沉淀:H2SiO3
SiO2+H2O,与题意相符.Si和SiO2与HF溶液反应均生成SiF4,SiF4与盐酸不反应.因此A是Si,B是SiO2,C是Na2SiO3(或K2SiO3),D是H2O,E是H2SiO3,F是H2,a是NaOH(或KOH),以此解答该题.
a溶液是强碱(如NaOH)溶液或HF溶液,而Si和SiO2与NaOH溶液反应均生成Na2SiO3.Na2SiO3与过量盐酸反应生成NaCl和H2SiO3白色沉淀:H2SiO3
| ||
解答:
解:A是一种固体单质,且常作半导体材料,A应为Si,F是最轻的气体单质,应为H2,a溶液是强碱(如NaOH)溶液或HF溶液,而Si和SiO2与NaOH溶液反应均生成Na2SiO3.Na2SiO3与过量盐酸反应生成NaCl和H2SiO3白色沉淀:H2SiO3
SiO2+H2O,与题意相符.Si和SiO2与HF溶液反应均生成SiF4,SiF4与盐酸不反应.因此A是Si,B是SiO2,C是Na2SiO3(或K2SiO3),D是H2O,E是H2SiO3,F是H2,a是NaOH(或KOH),
(1)由以上分析可知B是SiO2,目前在现代通讯方面已被用作光导纤维的主要材料,故答案为:SiO2;光导纤维;
(2)SiO2与NaOH(或KOH)溶液反应的离子方程式是SiO2+2OH-=SiO32-+H2O,故答案为:SiO2+2OH-=SiO32-+H2O;
(3)C是Na2SiO3(或K2SiO3),Na2SiO3(或K2SiO3)和过量盐酸反应生成硅酸沉淀,离子反应方程式为:SiO32-+2H+=H2SiO3↓,
故答案为:SiO32-+2H+=H2SiO3↓.
| ||
(1)由以上分析可知B是SiO2,目前在现代通讯方面已被用作光导纤维的主要材料,故答案为:SiO2;光导纤维;
(2)SiO2与NaOH(或KOH)溶液反应的离子方程式是SiO2+2OH-=SiO32-+H2O,故答案为:SiO2+2OH-=SiO32-+H2O;
(3)C是Na2SiO3(或K2SiO3),Na2SiO3(或K2SiO3)和过量盐酸反应生成硅酸沉淀,离子反应方程式为:SiO32-+2H+=H2SiO3↓,
故答案为:SiO32-+2H+=H2SiO3↓.
点评:本题考查无机物的推断,解答本题的关键是A为固体单质,E为白色沉淀,本题的突破口是C加入过量盐酸生成白色沉淀E,容易想到E为H2SiO3,题目难度不大.

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、非金属单质分子中一定含有非极性共价键 | ||||
| B、根据电离方程式:HCl=H++Cl-,判断HCl分子中存在离子键 | ||||
C、根据2C+SiO2
| ||||
| D、变化过程中化学键被破坏,不一定发生了化学变化 |
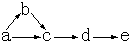 如图a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:其中:a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物.已知H2S在足量氧气中燃烧生成SO2.
如图a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:其中:a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物.已知H2S在足量氧气中燃烧生成SO2.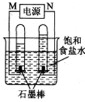
 Ⅰ.在一定条件下的下列可逆反应达到平衡时,试填出:x A+y B?z C
Ⅰ.在一定条件下的下列可逆反应达到平衡时,试填出:x A+y B?z C