题目内容
按下列要求写出由第二周期非金属元素组成的中性分子的相关内容:
(1)平面三角形分子:分子式_____________,中心原子杂化方式是___________________。
(2)三角锥形分子:分子式______________,VSEPR模型为 。
(3)正四面体形分子:结构式______________,中心原子杂化方式是__________________。
(4)互为等电子体的两对物质的分子式:N2和_____________,CO2和_________________。
(1)平面三角形分子:分子式_____________,中心原子杂化方式是___________________。
(2)三角锥形分子:分子式______________,VSEPR模型为 。
(3)正四面体形分子:结构式______________,中心原子杂化方式是__________________。
(4)互为等电子体的两对物质的分子式:N2和_____________,CO2和_________________。
(1)BF3 SP2 (2)NF3 四面体形
(3)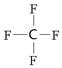 SP3 (4)CO N2O
SP3 (4)CO N2O
(3)
 SP3 (4)CO N2O
SP3 (4)CO N2O试题分析:在第二周期元素形成的分子中,属于平面三角形的是BF3,中心原子没有孤对电子,所以是sp2杂化;属于三角锥形的是氨气,中心原子氮原子含有(5-3×1)÷2=1,所以VSEPR模型为四面体型;属于正四面体型结构的是四氟化碳,结构式是
 ,中心原子没有孤对电子,属于sp3杂化;原子数和价电子数分别都相等的是等电子体,所以和 互为等电子体的是CO,和CO2互为等电子体的是N2O。
,中心原子没有孤对电子,属于sp3杂化;原子数和价电子数分别都相等的是等电子体,所以和 互为等电子体的是CO,和CO2互为等电子体的是N2O。点评:该题是中等难度的试题,也是高考中的常见题型和重要的考点。试题紧扣教材,难易适中,基础性强。旨在培养学生灵活运用基础知识甲基实际问题的能力,有利于培养学生的逻辑推理能力和创新思维能力。

练习册系列答案
相关题目
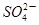 和
和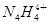 两种离子,当
两种离子,当
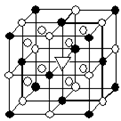

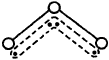
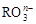 和I-发生反应的离子方程式为:
和I-发生反应的离子方程式为: