题目内容
O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图,呈V型,键角116.5℃。三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子。请回答:
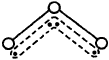
O3的分子结构
(1)臭氧与氧气的关系是___________。
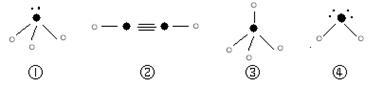
(2)选出下列分子中与O3分子属于等电子体的是 。
(3)分子中某原子有1对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有_______ 对孤对电子。
(4)O3与O2间的转化是否为氧化还原反应___________。

O3的分子结构
(1)臭氧与氧气的关系是___________。
(2)选出下列分子中与O3分子属于等电子体的是 。
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(4)O3与O2间的转化是否为氧化还原反应___________。
(1)同素异形体 (2)C (3)5 (4)否
试题分析:(1)臭氧与氧气都是氧元素形成的不同单质,二者互为同素异形体。
(2)原子数和价电子数分别都相等的是等电子体,则与O3分子属于等电子体的是二氧化硫,答案选C。
(3)根据臭氧的结构和孤对电子的含义可知,臭氧分子中含有的孤对电子有2+1+2=5对。
(4)O3与O2是两种不同的单质,二者之间的转化是化学变化,但没有电子的得失,所以不是氧化还原反应。
点评:该题是基础性试题的考查,难度不大。试题贴近高考,基础性强,有利于调动学生的学习兴趣和学习积极性,也有助于培养学生的逻辑推理能力和发散思维能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 ,在S—N键,你认为该共用电子对偏向于________原子(填元素符号)。
,在S—N键,你认为该共用电子对偏向于________原子(填元素符号)。 与互为等电子体,O22+的电子式可表示为 ;
与互为等电子体,O22+的电子式可表示为 ; ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“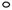 ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键。
”表示没有形成共价键的最外层电子,短线表示共价键。