题目内容
【题目】下列有关如图有机物说法正确的是
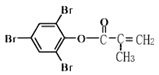
A.有机物中所有原子均在同一平面内
B.可发生的反应类型有取代、加成、还原、水解、氧化
C.1 mol 该化合物最多能与含5 mol NaOH的溶液反应
D.既能使酸性KMnO4 溶液褪色,又能与FeCl3溶液发生显色反应
【答案】B
【解析】
A.该分子中含有1个-CH3,其空间结构类似于CH4,为四面体结构,不可能所有原子共平面,A错误;
B.溴原子和酯基可发生取代反应、水解反应,碳碳双键和苯环可与H2发生加成,也是还原反应,碳碳双键能被高锰酸钾等氧化,能发生氧化反应;该有机物可以燃烧,也是氧化反应,B正确;
C.酯基水解生成的酚羟基、羧基;溴原子水解生成的酚羟基、HBr都能和NaOH反应,则1mol该化合物最多能与含8molNaOH的溶液反应,C错误;
D.分子中含有碳碳双键,能使高锰酸钾溶液褪色;但没有酚羟基,不能和氯化铁溶液发生显色反应,D错误。
答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】实验室制备纯碱的主要步骤如流程所示:

四种盐在不同温度下的溶解度(g/100gH2O)表
温度 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | - | - | - | - |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
提示:温度高于35℃时NH4HCO3会分解,请回答:
(1)下列操作或描述正确的是________。
A.温度控制在30-35℃是因为温度太高NH4HCO3会分解,温度太低反应速率太慢
B.保温30min的目的是使反应充分进行
C.过滤后的滤液只有NH4Cl和NH4HCO3溶质
D.洗去晶体表面的杂质可以选用蒸馏水
(2)反应温度控制在30~35℃,为控制此温度范围,采取的加热方法为______________。
(3)常温时,过滤后主要得到NaHCO3晶体的原因是______________。
(4)灼烧NaHCO3晶体的装置为________。
A.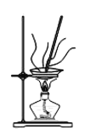 B.
B.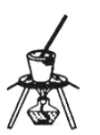 C.
C.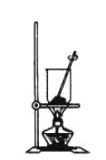
(5)洗涤NaHCO3晶体的操作______________。
(6)测定纯碱产品中NaHCO3含量的方法:准确称取纯碱样品Wg放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用物质的量浓度为c(mol·L-1)的HCl溶液滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点)所用HCl溶液体积为V1mL。再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液体积为V2mL,写出纯碱样品中NaHCO3质量分数的计算式:______________。