题目内容
16.硫醇-烯具有反应过程相对简单、反应过程可控等优点,成为近年来有机合成的研究热点之一,如反应①
(1)化合物I的分子式为C7H8S,反应①的反应类型为加成反应.
(2)化合物Ⅱ与Br2加成的产物的结构简式为
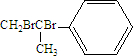 ,化合物Ⅱ完全燃烧消耗O211.5 mol.
,化合物Ⅱ完全燃烧消耗O211.5 mol.(3)化合物Ⅲ的氧化产物化合物Ⅳ能发生银镜反应,则Ⅲ的结构简式为
 .化合物Ⅳ与新制Cu(OH)2反应的化学方程式
.化合物Ⅳ与新制Cu(OH)2反应的化学方程式 .
.(4)化合物Ⅲ的一种同分异构体Ⅴ能与碳酸钠溶液反应,且核磁共振氢谱显示Ⅴ中存在5组峰,峰面积之比为1:1:2:2:6,化合物Ⅴ的结构简式为
 .
.(5)一定条件下CH3CH2SH与
 能发生类似反应①的反应经两步生成化合物Ⅶ,Ⅶ的结构简式为
能发生类似反应①的反应经两步生成化合物Ⅶ,Ⅶ的结构简式为 .
.
分析 (1)由化合物I的结构简式确定元素种类和原子个数可确定有机物分子式,对比结构简式,反应①的特点是碳碳双键变成单键;
(2)化合物Ⅱ含有碳碳双键,可与溴发生加成反应;根据化合物Ⅱ的结构简式写出其分子式,再计算出1mol该有机物完全燃烧消耗氧气的物质的量;
(3)化合物Ⅲ的氧化产物化合物Ⅳ能发生银镜反应,说明Ⅳ含有醛基,则Ⅲ应含有-CH2OH基团;醛基可在加热条件下被氢氧化铜浊液氧化;
(4)能够与碳酸钠溶液反应、分子中只含有1个O,则该有机物分子中含有1个酚羟基,再结合核磁共振氢谱判断V的结构简式;
(5)反应①为化合物Ⅰ中的S-H键与化合物Ⅱ中碳碳双键发生加成,且化合物Ⅰ中的氢加在碳碳双键氢少的碳上,据此判断Ⅶ的结构简式.
解答 解:(1)根据化合物I的结构简式可知,该有机物分子式为:C7H8S;对比结构简式,反应①的特点是碳碳双键变成单键,应为加成反应,
故答案为:C7H8S;加成反应;
(2)化合物Ⅱ含有碳碳双键,可与溴发生加成反应,生成物结构简式为: ;
;
化合物Ⅱ的分子式为:C9H10,1mol该有机物完全燃烧消耗氧气的物质的量为:(9+$\frac{10}{4}$)mol=11.5mol,
故答案为: ;11.5;
;11.5;
(3)化合物Ⅲ的氧化产物化合物Ⅳ能发生银镜反应,说明Ⅳ含有醛基,则Ⅲ应含有-CH2OH基团,化合物Ⅲ的为: ,
,
故化合物Ⅳ为 ,
, 与新制Cu(OH)2反应的化学方程式为:
与新制Cu(OH)2反应的化学方程式为: ,
,
故答案为: ;
; ;
;
(4)化合物Ⅲ的一种同分异构体Ⅴ能与碳酸钠溶液反应,由于其分子中只含有1个O原子,则化合物V分子中一定含有酚羟基;
核磁共振氢谱显示存在5组峰,峰面积之比为1:1:2:2:6,该有机物分子中应该含有两个甲基,且具有对称结构,
所以化合物V的结构简式为: ,
,
故答案为: ;
;
(5)反应①为化合物Ⅰ中的S-H键与化合物Ⅱ中碳碳双键发生加成,且化合物Ⅰ中的氢加在碳碳双键氢少的碳上,则一定条件下CH3CH2SH与 能发生类似反应①的反应经两步生成化合物Ⅶ,Ⅶ的结构简式为:
能发生类似反应①的反应经两步生成化合物Ⅶ,Ⅶ的结构简式为: ,
,
故答案为: .
.
点评 本题考查有机物的合成,为高频考点,题目难度中等,涉及烯烃的性质、烃的燃烧耗氧量计算、醇催化氧化规律、醛的还原性、结构简式推断、方程式书写等知识,试题侧重于学生的分析能力的考查,熟练掌握官能团的性质与转化为解答关键.

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案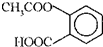 ,则1摩尔阿斯匹林和足量Na.H溶液充分反应,消耗NaOH的物质的量为( )
,则1摩尔阿斯匹林和足量Na.H溶液充分反应,消耗NaOH的物质的量为( )| A. | 1 mol | B. | 2 mol | C. | 3 mol | D. | 4 mol |
| A. | C2H6和C2H4 | B. | CH3CH2Cl和CH3CH2CH2CCl3 | ||
| C. | CH3CH2CH3和C5H12 | D. | CH3CH2CH2OH和HOCH2CH2OH |
| A. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出溴 | |
| B. | 乙烷中混有乙烯,通H2在一定条件下反应,使乙烯转化为乙烷 | |
| C. | 硝基苯中混有浓H2SO4和浓HNO3,将其倒入NaOH溶液中,静置,分液 | |
| D. | 乙烯中混有CO2和SO2,将其通过盛有NaOH溶液的洗气瓶 |

| A. | 1mol该有机物最多能与含2mol Br2的水溶液反应 | |
| B. | A的核磁共振氢谱图上有7个吸收峰 | |
| C. | A能发生银镜反应和酯化反应 | |
| D. | 与足量NaOH溶液反应转变成 |
| A. | 该元素的原子最外层上有6个电子 | |
| B. | 该元素最高价氧化物的化学式为RO2 | |
| C. | 该元素是非金属元素 | |
| D. | 该元素最高价含氧酸的化学式为H2RO4 |
| A. | 淀粉(氯化钠)渗析 | |
| B. | 硬脂酸钠(甘油溶液)盐析、过滤 | |
| C. | 水(鸡蛋清)蒸馏 | |
| D. | 蔗糖(葡萄糖)与银氨溶液混合水浴加热,过滤 |
| A. | 酸性:H4SiO4<H3PO4<H2SO4<HClO4 | B. | 碱性:Ca(OH)2>Mg(OH)2>Al(OH)3 | ||
| C. | 氢化物的稳定性:SiH4>H2S>H2O>HF | D. | 原子半径:F<O<S<Na |
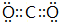 ,Y可形成分子晶体.过量的Y与氢氧化钠反应后的丁溶液与甲和氢氧化钠反应后的戊溶液发生的离子反应为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-.
,Y可形成分子晶体.过量的Y与氢氧化钠反应后的丁溶液与甲和氢氧化钠反应后的戊溶液发生的离子反应为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-.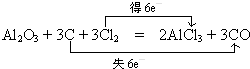 .
.