题目内容
14.下列叙述正确的是( )| A. | 稀醋酸中加入少量醋酸钠固体能增大醋酸的电离程度 | |
| B. | 25℃时,等体积等浓度的硝酸与氨水混合后,溶液呈中性 | |
| C. | 25℃时,0.1mol•L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 | |
| D. | FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 |
分析 A.加入醋酸钠,溶液中醋酸根离子浓度增大,抑制醋酸的电离;
B.25℃时,等体积等浓度的硝酸与氨水混合后为NH4NO3溶液,溶液中铵根离子水解,溶液呈酸性;
C.硫化氢为弱电解质,而硫化钠为强电解质,等浓度溶液中硫化氢溶液中离子浓度远远小于硫化钠溶液中离子浓度;
D.不同的催化剂催化效果不同.
解答 解:A.稀醋酸溶液中存在平衡:CH3COOH?CH3COO-+H+,加入醋酸钠,溶液中CH3COO-离子浓度增大,抑制醋酸的电离,故A错误;
B.25℃时,等体积等浓度的硝酸与氨水混合后为NH4NO3溶液,溶液中铵根离子水解,溶液呈酸性,故溶液pH<7,故B错误;
C.硫化氢为弱电解质,部分电离,而硫化钠为强电解质,等浓度溶液中硫化氢溶液中离子浓度远远小于硫化钠溶液中离子浓度,硫化氢溶液比等浓度的硫化钠溶液的导电能力弱,故C正确;
D.不同的催化剂的催化效果不一定相同,所以同等条件下二者对H2O2分解速率的改变不一定相同,故D错误,
故选C.
点评 本题考查弱电解质的电离平衡以及催化剂对反应速率的影响,难度不大,A为易错点,学生容易认为醋酸根与氢离子结合,平衡右移,促进电离.

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
10.在某溶液中加入AgNO3溶液,再加入稀硝酸,有白色沉淀出现,则该溶液 ( )
| A. | 必定是可溶性氯化物 | B. | 可能是可溶性碳酸盐 | ||
| C. | 可能含有Cl- | D. | 必定是氯水 |
5.300℃时,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:
回答下列问题:
(1)反应0~2min Z的平均速率v(Z)=0.004 mol/(L•min)
(2)能判断该反应已经达到平衡状态的是D
A.生成X的速率是生成Z的速率的2倍 B.容器内压强保持不变
C.容器内气体的密度保持不变 D.容器内各气体的浓度保持不变
(3)要提高上述反应的转化率,可采取的措施是降低温度(任写一种).
(4)温度为300℃时,该反应的化学平衡常数K=1.44
(5)若起始时向该容器中充入X、Y、Z各0.20mol,则反应将向正(填“正”或“逆”)反应方向进行,达平衡时Z的体积分数与上述平衡相比不变(填“增大”、“减小”或“不变”)
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
(1)反应0~2min Z的平均速率v(Z)=0.004 mol/(L•min)
(2)能判断该反应已经达到平衡状态的是D
A.生成X的速率是生成Z的速率的2倍 B.容器内压强保持不变
C.容器内气体的密度保持不变 D.容器内各气体的浓度保持不变
(3)要提高上述反应的转化率,可采取的措施是降低温度(任写一种).
(4)温度为300℃时,该反应的化学平衡常数K=1.44
(5)若起始时向该容器中充入X、Y、Z各0.20mol,则反应将向正(填“正”或“逆”)反应方向进行,达平衡时Z的体积分数与上述平衡相比不变(填“增大”、“减小”或“不变”)
19.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | 根据是否具有丁达尔效应,将分散系分为溶液、浊液、胶体 | |
| D. | 工业上电解熔融的MgCl2,可制得金属镁 |
4.下列说法正确的是( )
| A. | 某物质经测定,只含有一种组成元素,则该物质一定是单质 | |
| B. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| C. | 碱性氧化物均是金属氧化物,酸性氧化物均是非金属氧化物 | |
| D. | 纯净的硫酸是纯净物,而纯净的盐酸是混合物 |
 .
.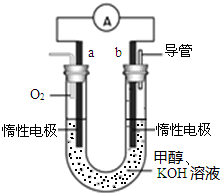 (1)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是b
(1)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是b
 .
.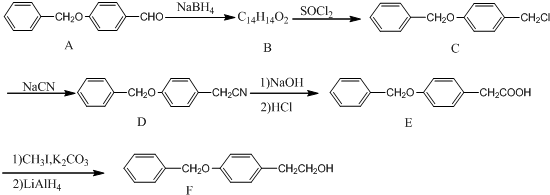
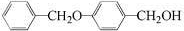 ;由A→B的反应类型是:还原反应.
;由A→B的反应类型是:还原反应.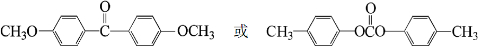 .
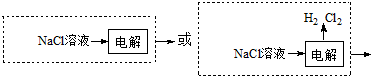
. 为原料制备化合物X(
为原料制备化合物X(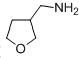 )(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
)(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如下: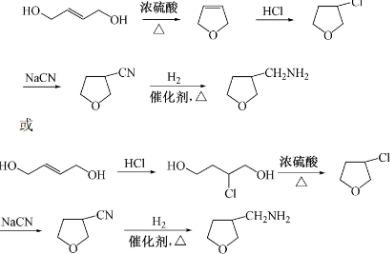 .
.