题目内容
5.A、B、C、D为原子序数依次增大的四种短周期元素,其性质或结构信息如下表:| 元素 | A | B | C | D | E |
| 性质 或结 构信 息 | 室温下单质呈气态,原子最外层电子数与D相同 | D3B中阳离子与阴离子的电子层结构相同 | A和C可形成两种常见的化合物甲和乙,甲有强氧化性 | 单质质软、银白色固体、导电性强,在空气中燃烧生成淡黄色固体 | E的气态氢化物和最高价氧化物对应的水化物均为强酸,C、D和E三种元素形成的一种盐丙为某消毒液的主要成分 |
(1)B在周期表中的位置是第二周期第ⅤA族,B的氢化物与E的氢化物比较,沸点较高的是NH3(填化学式).
(2)D3B可与水反应生成2种碱性物质,请写出这一化学方程式Na3N+3H2O=3NaOH+NH3↑.
(3)写出丙的电子式为
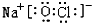 .丙在水溶液中的电离方程式NaClO=Na++ClO-.
.丙在水溶液中的电离方程式NaClO=Na++ClO-.(4)由B、C、D三种元素组成的一种盐丁,其外观与氯化钠相似,丁的水溶液呈中性.将光亮的铜丝插入丁溶液中,没有现象发生,如用盐酸酸化,反应迅速发生,铜丝缓慢溶解生成蓝色溶液,写出该反应的离子方程式3Cu+8H++2=3Cu2++2NO↑+4H2O.
分析 A、B、C、D为原子序数依次增大的四种短周期元素,D单质质软、银白色固体、导电性强,在空气中燃烧生成淡黄色固体,则D为Na;室温下A单质呈气态,原子最外层电子数与D相同,则A为H元素;D3B中阳离子与阴离子的电子层结构相同,离子核外电子数为10,故B原子核外电子数为10-3=7,故B为N元素;A和C可形成两种常见的化合物甲和乙,甲有强氧化性,结合原子序数可知,C为O元素,则甲为H2O2、乙为H2O;E的气态氢化物和最高价氧化物对应的水化物均为强酸,C、D和E三种元素形成的一种盐丙为某消毒液的主要成分,则E为Cl,丙为NaClO,据此解答.
解答 解:A、B、C、D为原子序数依次增大的四种短周期元素,D单质质软、银白色固体、导电性强,在空气中燃烧生成淡黄色固体,则D为Na;室温下A单质呈气态,原子最外层电子数与D相同,则A为H元素;D3B中阳离子与阴离子的电子层结构相同,离子核外电子数为10,故B原子核外电子数为10-3=7,故B为N元素;A和C可形成两种常见的化合物甲和乙,甲有强氧化性,结合原子序数可知,C为O元素,则甲为H2O2、乙为H2O;E的气态氢化物和最高价氧化物对应的水化物均为强酸,C、D和E三种元素形成的一种盐丙为某消毒液的主要成分,则E为Cl,
(1)B为N元素,在周期丙为NaClO,表中的位置是:第二周期第ⅤA族;B、E的氢化物分别为NH3、HCl,氨气分子之间存在氢键,沸点高于HCl,
故答案为:第二周期第ⅤA族;NH3;
(2)Na3N可与水反应生成2种碱性物质,生成氢氧化钠与氨气,该反应化学方程式为:Na3N+3H2O=3NaOH+NH3↑,
故答案为:Na3N+3H2O=3NaOH+NH3↑;
(3)丙为NaClO,电子式为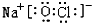 ,丙在水溶液中的电离方程式为:NaClO=Na++ClO-,
,丙在水溶液中的电离方程式为:NaClO=Na++ClO-,
故答案为: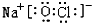 ;NaClO=Na++ClO-;
;NaClO=Na++ClO-;
(4)由N、O、Na三种元素组成的一种盐丁,其外观与氯化钠相似,丁的水溶液呈中性,则丁为NaNO3,将光亮的铜丝插入丁溶液中,没有现象发生,如用盐酸酸化,反应迅速发生,铜丝缓慢溶解生成蓝色溶液,该反应的离子方程式为:3Cu+8H++2=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2=3Cu2++2NO↑+4H2O.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,需要学生具备扎实的基础,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | MnO4-、Fe2+、K+、Cl- | B. | Ca2+、Na+、Cl-、SO42- | ||
| C. | Ca2+、Cl-、NO3-、K+ | D. | Ca2+、H+、OH-、CO32- |
| A. | CH3CH2OH→CH2=CH2↑+H2O | |
| B. | CH3CHBrCH3+NaOH→CH3CH=CH2↑+NaBr+H2O | |
| C. |  CHClCH2Cl+2NaOH→ CHClCH2Cl+2NaOH→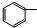 C≡CH+2NaCl+2H2O C≡CH+2NaCl+2H2O | |
| D. | 2CH3OH→CH3-O-CH3+H2O |
| A. | 锗是一种金属性很强的元素 | B. | 锗化氢(GeH4)稳定性很强 | ||
| C. | 锗酸(H4GeO4)是难溶于水的强酸 | D. | 锗元素位于第四周期第ⅣA族 |
| A. | 若XY3分子中X原子处于正三角形的中心,则XY3分子为非极性分子 | |
| B. | C2H5OH与C2H5Br相比,前者的沸点远高于后者,其原因是前者的分子间存在氢键 | |
| C. | 同周期ⅠA族元素和ⅦA族元素之间只能形成离子化合物 | |
| D. | 由两种非金属元素组成的化合物分子中只可能有极性键,不会有非极性键 |
| A. | 浓硫酸的稀释 | B. | 铝热反应 | ||
| C. | 氢气还原氧化铜 | D. | 氢氧化钡晶体与氯化铵晶体混合 |
| A. | ${\;}_{88}^{226}$Ra原子核内有138个中子 | B. | ${\;}_{88}^{226}$Ra原子核外有88个电子 | ||
| C. | ${\;}_{88}^{226}$Ra原子核内有88个质子 | D. | Ra元素位于第六周期 |
| A. | 该有机物的分子式为CH4 | B. | 该有机物中含碳元素和氢元素 | ||
| C. | 该有机物中只含有碳元素和氢元素 | D. | 该有机物的化学性质比较稳定 |
| A. | 钠与硫酸铜溶液反应会置换出红色的铜 | |
| B. | 常温下干燥氯气与铁不反应,可以用钢瓶储存液氯 | |
| C. | CO2、NO2、SO2都能与H2O反应,其反应原理相同 | |
| D. | C、N、S三种单质直接与O2反应都能生成两种氧化物 |