题目内容
4.下列物质中,属于共价化合物的是( )| A. | MgCl2 | B. | H2SO4 | C. | NH4Cl | D. | NaOH |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,不同非金属元素之间易形成极性键,同种非金属元素之间易形成非极性键,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,只含共价键的化合物为共价化合物.
解答 解:A.MgCl2中只含离子键,为离子化合物,故A错误;
B.硫酸分子中只含共价键,是共价化合物,故B正确;
C.NH4Cl中既含离子键又含共价键,为离子化合物,故C错误;
D.氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在共价键,为离子化合物,故D错误;
故选B.
点评 本题考查了化学键和化合物的关系,明确离子化合物和共价键化合物的概念是解本题关键,注意:并不是所有的物质中都含有化学键,稀有气体中不含化学键,为易错点.

练习册系列答案
相关题目
15.现有A、B、C、D、E、F六种位于周期表前四周期元素,其原子序数依次增大,相关信息如表所示:
根据以上信息,回答下列问题:
(1)画出元素C的基态价电子排布图: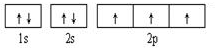 ;F元素位于周期表的d区;B、C、D三种元素的第一电离能由大到小顺序为:N>O>C(用元素符号表示).
;F元素位于周期表的d区;B、C、D三种元素的第一电离能由大到小顺序为:N>O>C(用元素符号表示).
(2)化合物BA2D2蒸气293K时,理论测算密度为2.0g•L-1,实际密度为2.5g•L-1的原因是甲酸形成分子间氢键.
(3)ED2中F原子的杂化类型为sp2; ED2易溶于水的原因可能是:①②(填入序号).
①ED2与水极性相同 ②ED2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为:离子键、共价键.
| 元素 | 性质 |
| A | 一种核素的原子核内不含中子 |
| B | 原子核外电子有6种不同运动状态 |
| C | 最高价氧化物的水化物与其氢化物可发生非氧化还原反应 |
| D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
| E | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
| F | 该元素的一种氧化物M可用作油漆颜料,与某单质反应可应用于焊接钢轨 |
(1)画出元素C的基态价电子排布图:
 ;F元素位于周期表的d区;B、C、D三种元素的第一电离能由大到小顺序为:N>O>C(用元素符号表示).
;F元素位于周期表的d区;B、C、D三种元素的第一电离能由大到小顺序为:N>O>C(用元素符号表示).(2)化合物BA2D2蒸气293K时,理论测算密度为2.0g•L-1,实际密度为2.5g•L-1的原因是甲酸形成分子间氢键.
(3)ED2中F原子的杂化类型为sp2; ED2易溶于水的原因可能是:①②(填入序号).
①ED2与水极性相同 ②ED2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为:离子键、共价键.
12.下列关于焰色反应的说法正确的是( )
| A. | 只有金属化合物才有焰色反应 | |
| B. | 焰色反应是化学变化 | |
| C. | 透过蓝色钴玻璃观察钾元素焰色反应的颜色为紫色 | |
| D. | 每次焰色反应实验后都要将铂丝蘸取氢氧化钠溶液洗涤并灼烧 |
19.下列反应属于吸热反应的是( )
| A. | 酸碱中和反应 | B. | 氢气的燃烧 | ||
| C. | 锌与硫酸反应 | D. | 碳与二氧化碳反应 |
16.常温下,下列关于NaOH溶液和氨水的说法正确的是( )
| A. | 相同物质的量浓度的两溶液中的c(OH-)相等 | |
| B. | pH=13的两溶液稀释100倍,pH都为11 | |
| C. | 两溶液中分别加入少量NH4Cl固体,c(OH-)均减小 | |
| D. | 体积相同、pH相同的两溶液能中和等物质的量的盐酸 |
13.洗涤盛放过植物油的试管,最宜选用的试剂是( )
| A. | 热水 | B. | 稀硫酸 | C. | 浓硝酸 | D. | 热NaOH溶液 |
6.已知氨水的浓度越大,密度越小.将质量分数为W%的氨水和质量分数为5W%的氨水等体积混合,所得溶液中氨的质量分数为( )
| A. | 6W% | B. | 3W% | C. | 大于3W% | D. | 小于3W% |
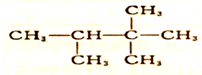 的系统命名为2,2,3-三甲基丁烷.
的系统命名为2,2,3-三甲基丁烷.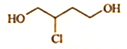 的分子式为C4H9O2Cl.
的分子式为C4H9O2Cl.