题目内容
【题目】芳香族化合物 E 是合成某种香料的中间体 ,以苯为原料合成 E 流程如下 :
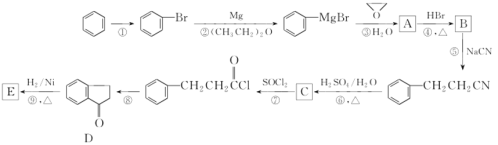
已知:CH3Br![]() CH3 MgBr
CH3 MgBr 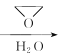 CH3CH 2CH2OH;
CH3CH 2CH2OH;
![]()
![]()
![]()
(1)写出反应①所需的试剂和条件______;
(2)化合物A中碳原子的杂化类型为_____, 分子中不同化学环境的氢原子共有___种;
(3)D中含氧官能团的名称为______;
(4)写出反应⑨的化学方程式_____,该反应的反应类型为_____;
(5)化合物C能与Na2CO3溶液反应生成CO2,符合以下 a 、b 、c、d条件的C的同分异构体与足量NaOH溶液反应的化学方程式___;
a.属于芳香族化合物 b.能发生银镜反应,也能发生水解反应 c. 结构中存在乙基 d苯环上的一氯代物只有 2 种
(6)以![]() 为主要原料,合成
为主要原料,合成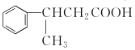 的流程为_________。
的流程为_________。
【答案】Br2/Fe(或Br2/FeBr3) sp2、sp3 6 羰基 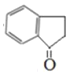 +H2
+H2![]()
 加成反应
加成反应 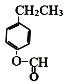 +2NaOH→
+2NaOH→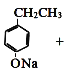 HCOONa+H2O
HCOONa+H2O ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
根据已知信息:CH3MgBr 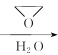 CH3CH2CH2OH;则
CH3CH2CH2OH;则![]() ,所以A是
,所以A是![]() ;
;![]() 与HBr发生取代反应生成B,B是
与HBr发生取代反应生成B,B是![]() ;
;![]() 在酸性条件下水解为羧酸C,C是
在酸性条件下水解为羧酸C,C是![]() ;
;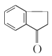 与氢气发生加成反应生成E,E是芳香族化合物,所以E的结构简式是
与氢气发生加成反应生成E,E是芳香族化合物,所以E的结构简式是 ,据此分析解答。
,据此分析解答。
(1)根据流程图示所示,反应①为苯与液溴用铁做催化剂,发生取代反应反应生成溴苯和溴化氢。所需的试剂和条件Br2/Fe(或Br2/FeBr3);
(2)A是![]() ,A中含有苯环为平面结构,苯环上的碳原子的杂化类型为sp2杂化,与苯环相连的碳原子都是饱和碳原子,类似于甲烷的结构,-CH2CH2OH上的碳原子的杂化类型为sp3;A分子结构对称,所以共有6种不同化学环境的氢原子;
,A中含有苯环为平面结构,苯环上的碳原子的杂化类型为sp2杂化,与苯环相连的碳原子都是饱和碳原子,类似于甲烷的结构,-CH2CH2OH上的碳原子的杂化类型为sp3;A分子结构对称,所以共有6种不同化学环境的氢原子;
(3)D的结构简式为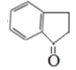 ,其中含氧官能团的名称是羰基;
,其中含氧官能团的名称是羰基;
(4)反应⑨为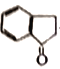 与氢气发生加成反应生成
与氢气发生加成反应生成 的化学方程式是
的化学方程式是 +H2
+H2![]()
 ;
;
(5)化合物C的同分异构体属于芳香族化合物,含有苯环;能发生银镜反应,也能发生水解反应,说明属于甲酸酯,存在乙基(-CH2CH3),且苯环上的一氯取代物只有两种,说明两个取代基位于苯环对位;符合条件的![]() 的同分异构体是
的同分异构体是 ,
, 与氢氧化钠反应的方程式是
与氢氧化钠反应的方程式是 +2NaOH→
+2NaOH→ HCOONa+H2O;
HCOONa+H2O;
(6)根据![]()
![]()
![]() ,
,![]() 可以先还原为
可以先还原为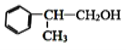 ,
,![]() 与溴化氢发生取代反应生成
与溴化氢发生取代反应生成![]() ,
,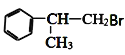 与NaCN反应生成
与NaCN反应生成 ,
, 在酸性条件下水解为
在酸性条件下水解为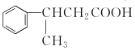 ,流程图为:
,流程图为:![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 。
。