题目内容
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g) +H2(g)![]() CO (g) +H2O (g)
CO (g) +H2O (g)
其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=__________。
(2)能说明该反应达到化学平衡状态的是________。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式: 3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为______℃。
(4) 830℃时,在1L密闭容器中分别投入lmolH2和lmolCO2反应达到化学平衡时,CO2的转化率为__________;保持温度不变,在平衡体系中再充入1molH2和lmolCO2重新达到化学平衡时,CO2的平衡转化率_________(填“增大”、“减小”或“不变”)。
【答案】 c(CO)c(H2O)/c(CO2)c(H2) B、C 700 50% 不变
【解析】(1)可逆反应CO2(g)+H2(g)CO(g)+H2O(g)的化学平衡常数表达式k=![]() ,故答案为:
,故答案为: ![]() ;
;
(2)能说明该反应达到化学平衡状态的是________。
A.该反应属于气体的物质的量不变的反应,容器中压强始终不变,不能说明该反应达到化学平衡状态,错误;B.混合气体中c(CO)不变,能说明该反应达到化学平衡状态,正确;
C.v正(H2)=v逆(H2O),表示正逆反应速率相等,能说明该反应达到化学平衡状态,正确;D.c(CO2)=c(CO),不能说明浓度是否变化,不能说明该反应达到化学平衡状态,错误;故选BC;
(3)平衡浓度符合下式3c(CO2)c(H2)=5c(CO)c(H2O)时,则![]() =
=![]() =0.6,平衡常数只值受温度的影响,当K=0.6时,根据表中数据,所以温度是700℃,故答案为:700;
=0.6,平衡常数只值受温度的影响,当K=0.6时,根据表中数据,所以温度是700℃,故答案为:700;
(4)令平衡时参加反应的CO2的物质的量为ymol,则:
CO2(g)+H2(g)CO(g)+H2O(g)
开始(mol): 1 1 00
变化(mol): yy yy
平衡(mol): 1-y1-yy y
故![]() =1,解得:y=0.5mol,故平衡后CO2的转化率为
=1,解得:y=0.5mol,故平衡后CO2的转化率为![]() ×100%=50%;保持温度不变,在平衡体系中再充入1molH2和lmolCO2重新达到化学平衡时,相当于增大压强,平衡不移动,CO2的平衡转化率不变,故答案为:50%,不变。
×100%=50%;保持温度不变,在平衡体系中再充入1molH2和lmolCO2重新达到化学平衡时,相当于增大压强,平衡不移动,CO2的平衡转化率不变,故答案为:50%,不变。

【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
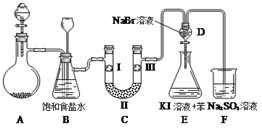
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:
___________________________________________________________。
(2)装置B中饱和食盐水的作用是_______________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入_______。
a | b | c | d | |
I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
II | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为______色,说明氯的非金属性大于溴。
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是_____________。
(6)有人提出,装置F中可改用足量的NaHSO3溶液吸收余氯,试写出相应的离子反应方程式:__________________,判断改用NaHSO3溶液是否可行______(填“是”或“否”)。