题目内容
【题目】由a、b、c、d四种金属按下表中装置进行实验。下列说法正确的是

A. 装置甲中化学能全部转化为电能
B. 装置乙中b电极发生的电极反应式为Cu2++2e-=Cu
C. 装置丙中SO42-向a电极移动,溶液的pH变小
D. 四种金属活动性由强到弱的顺序是b>e>d>a
【答案】B
【解析】甲装置中,金属b不断溶解说明该装置构成了原电池,且b失电子发生氧化反应而作负极,a作正极;乙中b的质量增加,说明b上铜离子得电子发生还原反应,则b作原电池正极,c作负极;丙装置中d上有气体产生,说明d上氢离子得电子发生还原反应,则d作原电池正极,a作负极,作原电池负极的金属活动性大于作正极金属,所以金属活动性强弱顺序是:c>b>a>d。
A. 装置甲为原电池,化学能转化为电能,但有部分转化为热能,故A错误;
B. 装置乙中b的质量增加,说明b上铜离子得电子发生还原反应,b电极发生的电极反应式为Cu2++2e-=Cu,故B正确;
C. 装置丙中a作负极,d作正极,SO42-向a电极移动,正极上发生反应:2H++2e-=H2↑,溶液的pH变大,故C错误;
D.通过以上分析,四种金属活动性由强到弱的顺序是c>b>a>d,故D错误;
所以B选项正确。

 通城学典默写能手系列答案
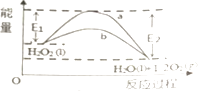
通城学典默写能手系列答案【题目】已知:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H 现在体积为1L的密闭容器中,充入CO2和H2 . 实验测得反应体系中物质的物质的量与时间关系如下表,
n(CO2) | n(H2) | n(CH3OH(g) | n(H2O(g) | |
0 | 1.00mol | 3.25mol | 0.00 | 0.00 |
5min | 0.50mol | 0.50mol | ||
10min | 0.25mol | 0.75mol | ||
15min | 0.25mol | n1 |
回答下列问题:
(1)表格中的n1=
(2)0﹣5min内 v (H2)=
(3)该条件下CO2的平衡转化率为 .
【题目】短周期p区元素共有13种,除铝外全部是非金属元素。
(1)基态氮原子的价层电子排布图为_______________;短周期p区元素中,第一电离能最小的元素与电负性最大的元素组成的化合物是_______________(填化学式)。
(2)卤素与硼、氮、磷可形成BF3,NCl3和PBr3。下列有关以上三种分子的叙述正确的是_________;
A.化学键类型相同 B.空间构型相同
C.中心原子的杂化轨道类型相同 D.中心原子的价层电子对数相同
(3)CS2是一种溶剂,它能溶解硫磺。写出一种与CS2具有相同空间构型和键合形式的分子或离子______________。CO能与Ni形成正四面体型的配合物Ni(CO)4,3.42gNi(CO)4中含有_____molσ键。
(4)CCl4与水互不相溶,SiCl4与CCl4分子结构相似,但遇水极易发生水解反应,导致二者性质不同的原因是________________。
(5)铝的几种卤化物的熔点如下:
卤化铝 | AlF3 | AlCl3 | AlBr3 | AlI3 |
熔点/℃ | 1040 | 190 | 97.5 | 191 |
AlBr3的晶体类型是______,AlI3晶体中存在的作用力有_______________。
(6)氮化铝晶体为原子品体,是一种新型无机非金属材料,其晶体密度为ɑg/cm3,晶胞如图所示。
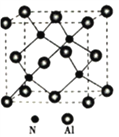
①铝原子的配位数为_______________。
②设NA为阿伏加德罗常数的值。氮化铝晶胞中,铝原子和氮原子之间最短的核间距为________nm。