题目内容
【题目】某草酸晶体的化学式可表示为H2C2O4xH2O,为测定x的值,进行下列实验: ①称取7.56g某草酸晶体配成100.0mL的水溶液,
②用移液管移取25.00mL所配溶液置于锥形瓶中,加入适量稀H2SO4 , 用浓度为0.600mol/L的KMnO4溶液滴定,滴定终点时消耗KMnO4 的体积为10.00mL.
(1)若滴定终点时仰视读数,则所测x的值将(填“偏大”或“偏小”).
(2)x= .
【答案】
(1)偏小
(2)2
【解析】解:(1)读取读数仰视,导致KMnO4溶液体积偏大,计算测定的草酸的质量偏大,故x的值偏小,所以答案是:偏小;(2)由题给化学方程式及数据可知,5H2C2O4+2MnO4﹣+6 H+═10CO2↑+2 Mn2++8 H2O,7.56g纯草酸晶体中含H2C2O4的物质的量为:0.600 mol/L×10.00 mL×10﹣3 L/mL× ![]() ×
× ![]() =0.0600 mol,则7.56g H2C2O4xH2O中含H2O的物质的量为
=0.0600 mol,则7.56g H2C2O4xH2O中含H2O的物质的量为 ![]() =0.12 mol,0.0600mol晶体含水0.160mol,1mol晶体中含的结晶水2mol,则x=2.
=0.12 mol,0.0600mol晶体含水0.160mol,1mol晶体中含的结晶水2mol,则x=2.
所以答案是:2.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】A、B、C、D、E、F是元素周期表前四周期中原子序数依次增大的六种常见元素,其相关信息如表:
元素 | 相 关 信 息 |
A | 原子核外有7种运动状态不同的电子 |
B | 外围电子排布式为nsnnpn+2 |
C | 常见的金属,在周期表中周期序数与族序数相等 |
D | 气态氢化物及最高价氧化物对应的水化物均为强酸 |
E | 一种核素的质量数为56,中子数为30 |
F | 单质紫红色,电缆材料,常见氧化物为黑色 |
回答下列问题:
(1)元素E在元素周期表中的位于第四周期第族,其高价态离子核外有个未成对电子
(2)B、C、D三种元素的离子半径由小到大的顺序是(用离子符号表示).
(3)A,D两元素的简单氢化物发生反应生成的化合物的电子式为
(4)常温下AD3是一种淡黄色液体.以下关于AD3的说法中,正确的是
A.AD3分子中只有非极性键
B.AD3分子中各原子均达8e﹣稳定结构
C.AD3的晶体属于分子晶体
D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是;该过程总的离子反应式为向反应后的溶液中加入适量乙醇,析出深蓝色晶体,该晶体中不含有的化学键类型是 A.配位键 B.极性共价键 C.非极性共价键 D.离子键.
【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO。反应的热化学方程式如下:
I.CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-53.7kJ·mol-1
CH3OH(g)+H2O(g) △H1=-53.7kJ·mol-1
I.CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
543 | Cat.l | 12.3 | 42.3 |
543 | Cat.2 | 10.9 | 72.7 |
553 | Cat.l | 15.3 | 39.1 |
553 | Cat.2 | 12.0 | 71.6 |
[备注]XCat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比。
已知:①CO和H2的标准燃烧热分别为-283.0kJ/mol和一285.8kJ/mol;
②H2O(l)==H2O(g) △H3=+44.0kJ·mol-1
请回答下列问题(不考虑温度对△H的影响):
(1)反应I在_________(填“低温”或“高温”)下自发进行;反应II每生成9g水蒸气放出热量为___________。
(2)恒容条件下,有利于提高CO2转化为CH3OH的平衡转化率的措施有_____(填字母代号)。
A.延长反应时间 B.使用催化剂Cat.2 C.降低反应温度
D.投料比不变,增加反应物的浓度 E.增大CO2和H2的初始投料比
(3)由表中实验数据可以得出的结论是_______________________。
(4)553K,使用催化剂Cat.2,在该时刻H2的转化率为______(填字母代号)。
A.5.5% B.13.3% C.16.4% D.29.3%
(5)在下图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程~能量”示意图。________
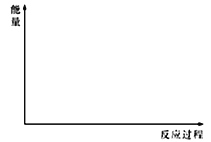
(6)研究证实,CO2也可在硫酸溶液中用情性电解生成甲醇,则生成甲醇的电极反应式是_________,另一极的电解产物为______________________。
【题目】表是25℃时四种酸的电离平衡常数:
化学式 | CH3COOH | HA | HNO2 | H2CO3 |
Ka | Ka=1.8×10﹣5 | Ka=4.9×10﹣10 | Ka=4.6×10﹣4 | Ka1 =4.1×10﹣7 |
(1)用离子方程式表示NaNO2溶液呈碱性的原因
(2)25℃时,向向0.1molL﹣1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO﹣)=5:9,此时溶液pH=
(3)写出NaA溶液中通少量CO2的离子方程式
(4)25℃时,等物质的量浓度的HA、NaA混合溶液呈碱性,溶液中各离子浓度的大小顺序为
(5)已知HNO2不稳定,在稀溶液中也易分解生成NO与NO2 , 某同学分别取少量NaCl溶液与NaNO2溶液于试管中,分别滴加浓醋酸,以此来鉴别失去标签的NaCl溶液和NaNO2溶液,该方法(填“可行”或“不可行”),理由是
(6)已知NaHCO3溶液中存在HCO3H++CO32﹣ , 加水稀释时溶液中的c(H+)将(填“增大”或“减小”)
【题目】常温下氨气能被氯气氧化成N2,化工厂常用浓氨水检验管道是否泄漏氯气。某兴趣小组在实验室对氨气与氯气反应进行了探究,回答下列问题:
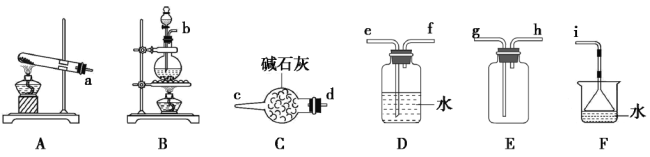
(1)氯气的发生装置可以选择上图中的_________(填大写字母),反应的离子方程式为________________。
(2)欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→________(按气流方向,用小写字母表示)。
II.氯气与氨气的反应
室温下,用收集到的氯气与氨气按下图所示装进行实验(实验前K1、K2关闭)。

(3)为使两种气体充分混合,气体a是___________(填化学式)。
(4)
操作步骤 | 实验现象 | 解释原因 |
打开K1,缓缓推动注射器活塞,向试 管中注入气体a (约是气体b的3倍), 关闭K1,恢复室温 | 试管内出现白烟并在 试管内壁凝结 | ①反应的化学方程式________ |
打开K2 | ②_________ | ③_________ |
