题目内容
13.下列各组化合物的水溶液中,碱的碱性减弱,酸的酸性增强的是( )| A. | NaOH,LiOH,HNO3,H3PO4 | B. | Mg(OH)2,Al(OH)3,HBrO4,HClO4 | ||
| C. | Mg(OH)2,Ca(OH)2,H3PO4,H2SO4 | D. | NaOH,Mg(OH)2,H3PO4,HClO4 |
分析 元素的非金属性越强,其最高价氧化物的水化物酸性越强,元素的金属性越强,其最高价氧化物的水化物碱性越强,据此分析解答.
解答 解:A.金属性Na>Li,所以碱性NaOH>LiOH;金属性N>P,所以酸性HNO3>H3PO4,故A错误;
B.金属性Mg>Al,碱性Mg(OH)2>Al(OH)3,非金属性Cl>Br,所以酸性HBrO4<HClO4,故B正确;
C.金属性Mg<Ca,所以碱性Mg(OH)2<Ca(OH)2,非金属性P<S,所以酸性H3PO4<H2SO4,故C错误;
D.金属性Na>Mg,所以碱性NaOH>Mg(OH)2,非金属性Cl>P,所以酸性H3PO4<HClO4,故D正确;
故选BD.
点评 本题考查酸碱性强弱判断,明确金属的金属性强弱与其碱的碱性强弱、非金属的非金属性强弱与其最高价含氧酸的酸性强弱关系是解本题关键,知道金属性、非金属性强弱判断方法,题目难度不大.

练习册系列答案
相关题目
6.在下列各溶液中,离子一定能大量共存的是( )
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ | |
| C. | 所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ | |
| D. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
4.向含有0.078mo l的FeCl2溶液中通入0.009molCl2,再加入含0.01molX2O72-的酸性溶液,使溶液中的Fe2+恰好全部氧化,并使X2O72-还原为Xn+,则n的值是( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
1.下列实验能获得成功的是( )
| A. | 苯和溴用铁作催化剂生成溴苯 | |
| B. | 向苯酚浓溶液中滴入少量浓溴水可观察到白色三溴苯酚沉淀 | |
| C. | 氯乙烷与NaOH溶液共热,在水解后的溶液中加入硝酸酸化的AgNO3溶液检验Cl- | |
| D. | 向淀粉在酸性条件下水解的产物中加银氨溶液,水浴加热,检验葡萄糖的生成 |
8.能用分液漏斗进行分离的一组物质是( )
| A. | 苯和硝基苯 | B. | 丙酸甲酯和水 | C. | 乙酸乙酯和乙酸 | D. | 溴苯和溴 |
18.下列有关说法中不正确的是( )
| A. | 将SO2通入BaCl2溶液中至饱和,无沉淀产生,再通入过量NH3,产生沉淀 | |
| B. | 高纯硅常用作光导纤维的原料 | |
| C. | 用AlCl3溶液制取Al(OH)3,沉淀剂选用氨水比选用NaOH溶液好 | |
| D. | 纯锌与稀硫酸反应产生氢气的速率较慢,再加入少量CuSO4固体,反应速率加快 |
5.下列化学用语表达正确的是( )
| A. | 一氯乙烷的结构式CH3Cl | B. | 丁烷的结构简式CH3(CH2)2CH3 | ||
| C. | 四氯化碳的电子式 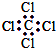 | D. | 苯的分子式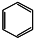 |
2.下列关于常见有机物的说法不正确的是 ( )
| A. | 食用植物油水解均可生成甘油 | |
| B. | 聚丙烯能使溴水褪色 | |
| C. | 苯和浓硝酸反应生成硝基苯,乙酸和乙醇反应生成乙酸乙酯,二者反应类型相同 | |
| D. | 向蔗糖水解后的溶液中加新制的Cu(OH)2悬浊液,加热到沸腾即可验证水解产物葡萄糖 |
3.中学化学中很多“规律”都可以类推,下列根据有关“规律”推出的结论正确的是( )
| A. | 硅是半导体材料,故同族的锗也是半导体材料 | |
| B. | 浓硫酸可以干燥HCl气体,故也可用浓硫酸干燥HI气体 | |
| C. | Na在空气中燃烧会生成Na2O2,故Li在空气中燃烧也会生成Li2O2 | |
| D. | 卤族元素单质随核电荷数增加熔点升高,故碱金属单质熔点也随核电荷数增加而升高 |