题目内容
8.能用分液漏斗进行分离的一组物质是( )| A. | 苯和硝基苯 | B. | 丙酸甲酯和水 | C. | 乙酸乙酯和乙酸 | D. | 溴苯和溴 |
分析 根据分液漏斗可以将互不相溶的两层液体分开,则分析选项中物质的溶解性即可.
解答 解:A.苯和硝基苯互溶,不能用分液的方法分离,故A错误;
B.丙酸甲酯和水不互溶,能分层,能用分液方法分离,故B正确;
C.乙酸乙酯和乙酸互溶,不能用分液的方法分离,故C错误;
D.溴苯和溴互溶,不能用分液的方法分离,故D错误.
故选B.
点评 本题考查了物质分离方法中的分液法,熟记物质的性质是解题的关键所在,难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
1.药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得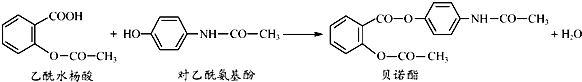
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A. | 贝诺酯分子中有三种含氧官能团 | |
| B. | 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应 | |
| C. | 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚 | |
| D. | 贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 |
2.如图所示,X、Y分别是直流电源的两极,通电后后发生a极板质量增加,b极板处有无色无味气体放出.符合这一情况的是( )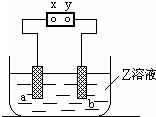

| a极板 | b极板 | X电极 | Z溶液 | |
| A | 石墨 | 石墨 | 正极 | NaOH |
| B | 铜 | 石墨 | 负极 | CuCl2 |
| C | 锌 | 石墨 | 负极 | CuSO4 |
| D | 银 | 铁 | 正极 | AgNO3 |
| A. | A | B. | B | C. | C | D. | D |
16.在一定条件下,可逆反应N2+3H2??2NH3(正反应是放热反应)达到平衡,当单独改变下列条件后,有关叙述错误的是( )
| A. | 加催化剂,v正、v逆都发生变化,且变化的倍数相等 | |
| B. | 加压,v正、v逆都增大,且v正增大的倍数大于v逆增大的倍数 | |
| C. | 降温,v正、v逆减小,且v正减小的倍数大于v逆减小的倍数 | |
| D. | 体积不变,加入氩气,v正、v逆都增大,且v正增大的倍数大于v逆增大的倍数 |
3.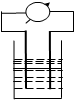 在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
 在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )| M | N | P | |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 铜 | 铁 | 硝酸铁溶液 |
| A. | A | B. | B | C. | C | D. | D |
13.下列各组化合物的水溶液中,碱的碱性减弱,酸的酸性增强的是( )
| A. | NaOH,LiOH,HNO3,H3PO4 | B. | Mg(OH)2,Al(OH)3,HBrO4,HClO4 | ||
| C. | Mg(OH)2,Ca(OH)2,H3PO4,H2SO4 | D. | NaOH,Mg(OH)2,H3PO4,HClO4 |
20.下列实验装置设计与对应结论正确的是( )
| 选项 | A | B | C | D |
| 装置 |  | 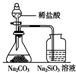 | 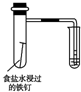 | 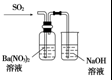 |
| 结论 | 能证明Al(OH)3不溶于氨水 | 能证明非金属性:Cl>C>Si | 验证铁发生析氢腐蚀 | 洗气瓶中产生的白色沉淀是BaSO3 |
| A. | A | B. | B | C. | C | D. | D |
17.如图为氢氧燃料电池原理示意图,下列叙述不正确的是( )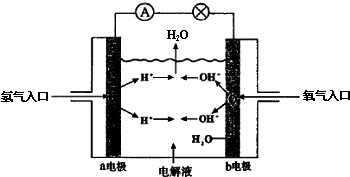

| A. | a电极是负极 | B. | b电极上发生氧化反应 | ||
| C. | 该电池工作时化学能转化为电能 | D. | 该电池的总反应为2H2+O2═2H2O |
18.下列离子方程式中正确的是( )
| A. | 少量SO2通入NaOH溶液中:OH-+SO2→HSO3- | |
| B. | H2S通入氯水中:S2-+Cl2→S↓+2Cl- | |
| C. | 二氧化氮溶于水:3NO2+H2O→2H++2NO3-+NO↑ | |
| D. | 少量NaHSO4与过量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-→BaSO4↓+2H2O |