��Ŀ����
 ���Ĺ̶���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol���ش��������⣺
���Ĺ̶���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol���ش��������⣺��1��д������ȼ���ȵ��Ȼ�ѧ����ʽ
��2���ں��º����ܱ������н��еĹ�ҵ�ϳɰ���Ӧ�������ܱ�ʾ�ﵽƽ��״̬����
A����������ѹǿ���ٷ����仯
B����������ƽ����Է����������ٷ����仯
C���������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮��
D����λʱ���ڶϿ�3a��H-H����ͬʱ�γ�6a��N-H��
E����Ӧ������N2��NH3�����ʵ����ı�ֵ���ٷ����仯
��3���ں��º��ݵ��ܱ������У���ҵ�ϳɰ���Ӧ�ĸ�����Ũ�ȱ仯������ͼ��ʾ����ش��������⣺
��ǰ25min�ڣ���N2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧƽ��������
����25minĩ��Ӧ�պôﵽƽ�⣬����¶��·�Ӧ��ƽ�ⳣ��K=
��4�������0.014mol/L��MgCl2��Һ��ͨ��һ�����İ�������Һ����仯���Բ��ƣ����������Һ��OH-��Ũ�ȴ���
��5��������PH=11�İ�ˮ��PH=3����������Һ�������ϣ�������Һ������Ũ�ȹ�ϵΪ
���㣺���ʵ�����Ũ����ʱ��ı仯����,�Ȼ�ѧ����ʽ,��ѧƽ��״̬���ж�,���������ˮ��Һ�еĵ���ƽ��
ר�⣺��ѧƽ��ר��
��������1����֪��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��
��N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol�����ø�˹���ɽ�
�ɵ�����ȼ�յ��Ȼ�ѧ����ʽ��
��2���ﵽƽ��ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�Դ�������һЩ������Ҳ���䣬�Դ��ж��Ƿ�ﵽƽ��״̬��
��3���ٸ���ͼ���е�Ũ�ȱ仯��ʱ��������N2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧƽ�����ʣ�
�ڸ���ƽ�ⳣ������ʽ������÷�Ӧ��ƽ�ⳣ���������¶ȣ�ƽ�������ƶ����÷�Ӧ��ƽ�ⳣ��ֵ����С��
��4�������ܶȻ��������㣻
��5��һˮ�ϰ�Ϊ������ʣ�������ȫ���룬������PH=11�İ�ˮ��PH=3����������Һ�������ϣ���ˮ��������Ӧ����Һ�ʼ��ԣ�
��N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol�����ø�˹���ɽ�
| �ڡ�2-�� |
| 6 |
��2���ﵽƽ��ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�Դ�������һЩ������Ҳ���䣬�Դ��ж��Ƿ�ﵽƽ��״̬��
��3���ٸ���ͼ���е�Ũ�ȱ仯��ʱ��������N2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧƽ�����ʣ�
�ڸ���ƽ�ⳣ������ʽ������÷�Ӧ��ƽ�ⳣ���������¶ȣ�ƽ�������ƶ����÷�Ӧ��ƽ�ⳣ��ֵ����С��
��4�������ܶȻ��������㣻
��5��һˮ�ϰ�Ϊ������ʣ�������ȫ���룬������PH=11�İ�ˮ��PH=3����������Һ�������ϣ���ˮ��������Ӧ����Һ�ʼ��ԣ�
���
�⣺��1����֪��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��
��N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol�����ø�˹���ɽ�
�ɵ�H2��g��+
O2��g��=H2O��l����H=-286.0 kJ/mol��
�ʴ�Ϊ��H2��g��+
O2��g��=H2O��l����H=-286.0 kJ/mol��
��2��A����������ѹǿ���ٷ����仯���ں��º����ܱ������У���Ϊ�ϳɰ������������Ŀ��С�ķ�Ӧ����������ѹǿ���ٷ����仯��˵���ﵽƽ��״̬����A��ȷ��
B����Ӧǰ����������ʵ�������ȣ�����������Է����������ٷ����仯����˵������������ʵ������䣬˵���ﵽƽ��״̬����B��ȷ��
C���������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮�ȣ��������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮�ȿ���ֻ��ijһʱ�̵ı�ֵ������֤���Ƿ�ﵽƽ�⣬��C����
D�������Ƿ�ﵽƽ��״̬�������ڵ�λʱ���ڶϿ�3a��H-H����ͬʱ�γ�6a��N-H��������˵���ﵽƽ��״̬����D����
E����Ӧ������N2��NH3�����ʵ����ı�ֵ���ٷ����仯��˵��������Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬����E��ȷ��
�ʴ�Ϊ��ABE��
��3����ͼ���е�����Ũ�ȵļ������������ٵ�
��CΪ������Ũ�ȱ仯���ߣ�
����ͼ���֪��v��N2��=
mol?L-1?min-1=0.04mol?L-1?min-1���ʴ�Ϊ��0.04 mol?L-1?min-1��
����25 min ĩ��Ӧ�պôﵽƽ�⣬K=
=
=
���÷�Ӧ�Ƿ��ȷ�Ӧ���������¶ȣ�ƽ�������ƶ����÷�Ӧ��ƽ�ⳣ��ֵ����С��
�ʴ�Ϊ��
����0.148��0.15��������
��4��Ksp[Mg��OH��2]=c��Mg2+����c2��OH-��=5.6��10-12����c��Mg2+��=0.014mol/L��
��c��OH-��=
mol/L=2��10-5mol/L��
�ʴ�Ϊ��2��10-5mol/L��
��5������ˮ��c��OH-������������c��H+����һˮ�ϰ���������ʣ��Ȼ�����ǿ����ʣ�����ˮŨ�ȴ������ᣬ���ߵ������ϣ���ˮ��������Һ�ʼ��ԣ���c��OH-����c��H+������Һ���ڵ���غ�c��NH4+��+c��H+��=c��Cl-��+c��OH-������c��NH4+����c��Cl-����ӦΪc��NH4+����c��Cl-����c��OH-����c��H+����
�ʴ�Ϊ��c��NH4+����c��Cl-����c��OH-����c��H+����
��N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol�����ø�˹���ɽ�
| �ڡ�2-�� |
| 6 |
| 1 |
| 2 |
�ʴ�Ϊ��H2��g��+
| 1 |
| 2 |
��2��A����������ѹǿ���ٷ����仯���ں��º����ܱ������У���Ϊ�ϳɰ������������Ŀ��С�ķ�Ӧ����������ѹǿ���ٷ����仯��˵���ﵽƽ��״̬����A��ȷ��
B����Ӧǰ����������ʵ�������ȣ�����������Է����������ٷ����仯����˵������������ʵ������䣬˵���ﵽƽ��״̬����B��ȷ��
C���������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮�ȣ��������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮�ȿ���ֻ��ijһʱ�̵ı�ֵ������֤���Ƿ�ﵽƽ�⣬��C����
D�������Ƿ�ﵽƽ��״̬�������ڵ�λʱ���ڶϿ�3a��H-H����ͬʱ�γ�6a��N-H��������˵���ﵽƽ��״̬����D����
E����Ӧ������N2��NH3�����ʵ����ı�ֵ���ٷ����仯��˵��������Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬����E��ȷ��
�ʴ�Ϊ��ABE��
��3����ͼ���е�����Ũ�ȵļ������������ٵ�
| 1 |
| 3 |
����ͼ���֪��v��N2��=
| 2.0-1.0 |
| 25 |
����25 min ĩ��Ӧ�պôﵽƽ�⣬K=
| c(NH3)2 |
| c(N2)?c(H2)3 |
| 4 |
| 1��33 |
| 4 |
| 27 |
�ʴ�Ϊ��
| 4 |
| 27 |
��4��Ksp[Mg��OH��2]=c��Mg2+����c2��OH-��=5.6��10-12����c��Mg2+��=0.014mol/L��
��c��OH-��=
|
�ʴ�Ϊ��2��10-5mol/L��
��5������ˮ��c��OH-������������c��H+����һˮ�ϰ���������ʣ��Ȼ�����ǿ����ʣ�����ˮŨ�ȴ������ᣬ���ߵ������ϣ���ˮ��������Һ�ʼ��ԣ���c��OH-����c��H+������Һ���ڵ���غ�c��NH4+��+c��H+��=c��Cl-��+c��OH-������c��NH4+����c��Cl-����ӦΪc��NH4+����c��Cl-����c��OH-����c��H+����
�ʴ�Ϊ��c��NH4+����c��Cl-����c��OH-����c��H+����
���������⿼����ۺϣ��漰֪ʶ��϶࣬�漰ͨ��ͼ�������ѧ��Ӧ���ʡ���ѧƽ�⼰���㡢���ܵ���ʵ��ܽ�ƽ���Լ�����Ũ�ȴ�С�Ƚϵ����⣬Ϊ��Ƶ���㣬������ѧ���ķ��������ͼ��������Ŀ��飬��Ҫѧ����ǿ�Ĺ۲�������˼ά�������ѶȽϴ�

��ϰ��ϵ�д�
 ȫ�ų��100��ϵ�д�
ȫ�ų��100��ϵ�д� Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д�
�����Ŀ
��NAΪ�����ӵ���������ֵ������������ȷ���ǣ�������
| A��1mol Cl2������Fe��Ӧת�Ƶ�����һ��Ϊ3NA |
| B����״���£�22.4L NH3�к��й��ۼ�����ĿΪNA |
| C��1.0L 1mol?L-1�Ĺ�����ˮ��Һ�к��е���ԭ����Ϊ3NA |
| D��4.6g Na��ȫת���������ƺ������ƵĻ��������������������Ϊ0.1NA |
ij��ɫ��Һ������Ƭ���������������ڸ���Һ����������һ�����Դ������ڵ��ǣ�������
| A��Na+ |
| B��Mg2+ |
| C��H+ |
| D��CO32- |
��ijNaOH��Һ��ͨ��CO2��������ҺM����CO2ͨ�����IJ�ͬ����ҺM�����Ҳ��ͬ������M����μ������ᣬ�������������V��CO2���������������V��HCl���Ĺ�ϵ����ͼ��ʾ����������ң�2������3������4��ͼ�зֱ���OA��AB��OA=AB��OA��AB�������з������жϲ���ȷ���ǣ�����CO2���ܽ⣩��������
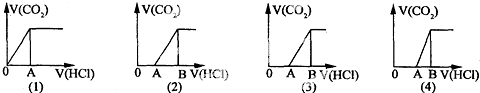

| A��M��ֻ��һ�����ʵ��У�1���ͣ�3�� |
| B��M�����������ʵ��У�2���ͣ�4�� |
| C����2��ͼ��ʾM�к���NaHCO3��Na2CO3�������� |
| D����4��ͼ��ʾM��c��NaHCO3����c��Na2CO3�� |
 ����ʳƷ���Ӽ�������ԭ�ϣ�����ζ�����ȩ����Ũ����
����ʳƷ���Ӽ�������ԭ�ϣ�����ζ�����ȩ����Ũ����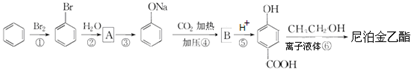
 ��
��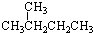 ��
��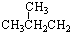 ��
��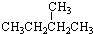

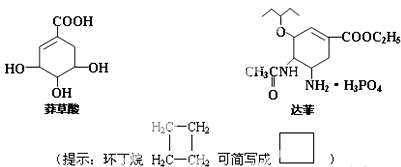
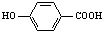 �����䷴Ӧ����Ϊ��
�����䷴Ӧ����Ϊ��