题目内容
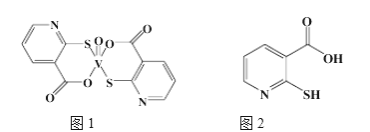
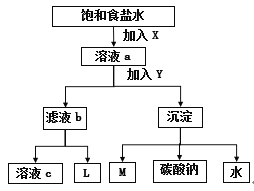
【题目】(1)砷(As)是一些工厂和矿山废水中的污染元素,使用吸附剂是去除水中砷的有效措施之一。将硫酸锰、硝酸钇与氢氧化钠溶液按一定比例混合,搅拌使其充分反应,可获得一种砷的高效吸附剂X,吸附剂X中含有![]() ,其原因是____________。
,其原因是____________。
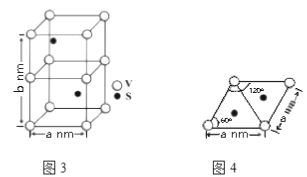
(2)H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题图1和题图2所示。
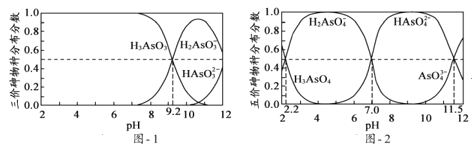
①以酚酞为指示剂(变色范围pH 8.0~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为____。
②H3AsO4第一步电离方程式H3AsO4![]() H2AsO4+H+的电离常数为Ka1,则pKa1=____(pKa1=-lgKa1)。
H2AsO4+H+的电离常数为Ka1,则pKa1=____(pKa1=-lgKa1)。
(3)25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是______。
A.0.1mol/L CH3COONa溶液与0.1mol/L HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-)
B.含等物质的量的NaX和弱酸HX的混合溶液中一定存在:c(Na+)>c(X-)
C.0.1mol/L Na2CO3溶液与0.1mol/L NaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3)
D.Na2C2O4溶液与HCl溶液等体积混合(H2C2O4是二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+)
(4)下列图示与对应的叙述不相符的是______。
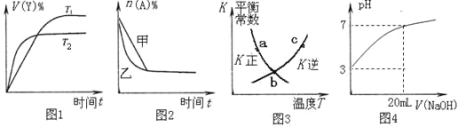
A.图1表示可逆反应“2X(g) ![]() Y(g)△H<0”温度T1<T2的情形
Y(g)△H<0”温度T1<T2的情形
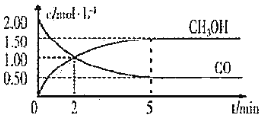
B.图2表示压强对可逆反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响,乙压强比甲压强大
3C(g)+D(s)的影响,乙压强比甲压强大
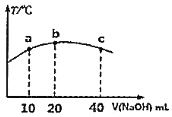
C.图3中a、b、c三点中只有b点已经达到化学平衡状态
D.图4是向20 mL pH=3的醋酸溶液中滴加pH=11的NaOH溶液过程中pH变化曲线
【答案】碱性溶液吸收了空气中的CO2 OH + H3AsO3=H2AsO3 + H2O 2.2 ACD BCD
【解析】
(1)空气中的CO2属于酸性氧化物,能溶于强碱溶液,NaOH是碱,能吸收空气中的二氧化碳而生成碳酸根离子,所以其原因是碱性溶液吸收了空气中的CO2;
(2)①根据图知,碱性条件下H3AsO3的浓度减小、H2AsO3-浓度增大,说明碱和H3AsO3生成H2AsO3-,该反应为酸碱的中和反应,同时还生成水,离子方程式为OH-+H3AsO3=H2AsO3-+H2O;
②Ka1=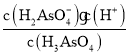 ,pH=2.2时c(H+)=10-2.2 mol/L,c(H3AsO3)=c(H2AsO3-),pKa1=-lgKa1=-lg
,pH=2.2时c(H+)=10-2.2 mol/L,c(H3AsO3)=c(H2AsO3-),pKa1=-lgKa1=-lg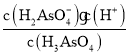 =2.2;
=2.2;
(3)A.溶液为氯化钠和醋酸混合溶液,且二者的物质的量浓度相等,混合溶液呈酸性,溶液中c(OH-)很小,且混合溶液中存在物料守恒,根据物料守恒得c(Na+)=c(Cl-),醋酸部分电离,所以溶液中存在c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-),故A正确;
B.等物质的量浓度、等体积的NaX和弱酸HX溶液混合后,溶液酸碱性情况取决于电离与水解的相对大小,无法确定溶液酸碱性,所以也无法比较各微粒物质的量浓度的大小,故B错误;
C.混合溶液存在物料守恒,根据物料守恒得:0.1molL-1 Na2CO3溶液中:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),0.1molL-1 NaHCO3溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),两式相加得,2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3),故C正确;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒得2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),故D正确;
故答案为ACD;
(4)A.由图可知,温度T2先到达平衡,故温度T1<T2,可逆反应2X(g) ![]() Y(g)△H<0,正反应为放热反应,升高温度平衡向逆反应移动,Y的含量降低,图象与实际相符合,故A正确;
Y(g)△H<0,正反应为放热反应,升高温度平衡向逆反应移动,Y的含量降低,图象与实际相符合,故A正确;
B.增大压强反应速率加快,平衡向正反应移动,平衡时A的物质的量降低,图象中到达平衡时间相同,且平衡时A的物质的量相同,图象与实际不符合,故B错误;
C.图象为正、逆平衡常数与温度关系,曲线上各点都是平衡点,故C错误;
D.20mLpH=3的醋酸溶液中滴加20mLpH=11的NaOH溶液,由于HAc是弱电解质,反应后为HAc、NaAc混合溶液,HAc浓度远大于NaAc,溶液呈酸性,图象中为中性,图象与实际不符,故D错误;
故答案为BCD。