题目内容
(14分)氢氟酸(HF)是一元弱酸,在水溶液中的电离方程式为:HF H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。
H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。

已知:电离度( )和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力,
)和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力, 。
。
请回答下列问题:
(1)在氢氟酸的稀溶液中,通过改变以下条件能使氢氟酸的电离度[ (HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_______。
(HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_______。
a.升高温度 b.向溶液中滴入2滴浓盐酸 c.加入少量NaF固体 d.加水稀释
(2)在此温度下,氢氟酸的电离平衡常数Ka(HF)为:__ (保留两位有效数字),电离度 约为___ _%。
约为___ _%。
(3)已知在此温度下:
H+(aq)+OH-(aq)=H2O(1) △H=-a kJ?mol -1;
HF(aq) H+(aq)+F-(aq) △H=+b kJ?mol -1
H+(aq)+F-(aq) △H=+b kJ?mol -1
则该过程中和反应的热化学方程式为:________________________________ ;在忽略F-水解的情况下,反应达到B点时,滴加过程中所释放的热量为________kJ(用只含a、b的式子表示)。
(4)下列有关图中各点微粒浓度关系正确的是_______________。
a.在A处溶液中:c(F—)+c(HF)="0.2" mol?L-1
b.在B处溶液中:c(H+)+c(HF)= c(OH—)
c.在B处溶液中:c(Na+)>c(F—)>c(H+)>c(OH—)
d.在A和B处溶液中都符合: = Ka(HF)
= Ka(HF)
 H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。
H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。
已知:电离度(
 )和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力,
)和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力, 。
。请回答下列问题:
(1)在氢氟酸的稀溶液中,通过改变以下条件能使氢氟酸的电离度[
 (HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_______。
(HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_______。a.升高温度 b.向溶液中滴入2滴浓盐酸 c.加入少量NaF固体 d.加水稀释
(2)在此温度下,氢氟酸的电离平衡常数Ka(HF)为:__ (保留两位有效数字),电离度
 约为___ _%。
约为___ _%。(3)已知在此温度下:
H+(aq)+OH-(aq)=H2O(1) △H=-a kJ?mol -1;
HF(aq)
 H+(aq)+F-(aq) △H=+b kJ?mol -1
H+(aq)+F-(aq) △H=+b kJ?mol -1则该过程中和反应的热化学方程式为:________________________________ ;在忽略F-水解的情况下,反应达到B点时,滴加过程中所释放的热量为________kJ(用只含a、b的式子表示)。
(4)下列有关图中各点微粒浓度关系正确的是_______________。
a.在A处溶液中:c(F—)+c(HF)="0.2" mol?L-1
b.在B处溶液中:c(H+)+c(HF)= c(OH—)
c.在B处溶液中:c(Na+)>c(F—)>c(H+)>c(OH—)
d.在A和B处溶液中都符合:
 = Ka(HF)
= Ka(HF)(1) a d(2分); a(2分) (2) 5.3×10-4(2分); 5(2分)
(3)HF(aq)+NaOH(aq)=" NaF(aq)+" H2O(l);△H=(b-a)kJ?mol-1(2分);0.004(a-0.95b)(2分) (4) b d(2分)
(3)HF(aq)+NaOH(aq)=" NaF(aq)+" H2O(l);△H=(b-a)kJ?mol-1(2分);0.004(a-0.95b)(2分) (4) b d(2分)
(1)电离是吸热的,所以a既能增大电离度,也能增大电离平衡常数。b是增大氢离子浓度,抑制电离,电离度减小,但电离平衡常数不变。C是增大氟离子浓度,抑制电离,电离度减小,但电离平衡常数不变。稀释促进电离,电离度增大,但电离平衡常数不变。所以答案分别选da和a。
(2)0.2mol?L-1的氢氟酸溶液中氢离子浓度是0.01mol/L,所以电离度是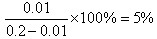 ,电离平衡常数为
,电离平衡常数为
(3)考查盖斯定律的应用。两式相加即得到HF(aq)+NaOH(aq)=" NaF(aq)+" H2O(l),所以反应热△H=(b-a)kJ?mol-1。反应达到B点时,二者恰好反应,生成0.004mol水和0.004molNaF。由于再反应中之前,HF已经有5%的发生了电离,所以实际放出的热量是0.004(a-0.95b)kJ。
(4)a不正确,因为溶液的体积已经不是20ml了。B正确,符合质子守恒。B点由于氟化钠水解显碱性,c不正确。D正确。符合电离平衡常数的表达式。答案选bd。
(2)0.2mol?L-1的氢氟酸溶液中氢离子浓度是0.01mol/L,所以电离度是
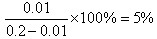 ,电离平衡常数为
,电离平衡常数为
(3)考查盖斯定律的应用。两式相加即得到HF(aq)+NaOH(aq)=" NaF(aq)+" H2O(l),所以反应热△H=(b-a)kJ?mol-1。反应达到B点时,二者恰好反应,生成0.004mol水和0.004molNaF。由于再反应中之前,HF已经有5%的发生了电离,所以实际放出的热量是0.004(a-0.95b)kJ。
(4)a不正确,因为溶液的体积已经不是20ml了。B正确,符合质子守恒。B点由于氟化钠水解显碱性,c不正确。D正确。符合电离平衡常数的表达式。答案选bd。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目