��Ŀ����
1��ʵ���Ҳ���MgCl2��AlCl3�Ļ����Һ�������ˮ��Ӧ�Ʊ�MgAl2O4����Ҫ�������£�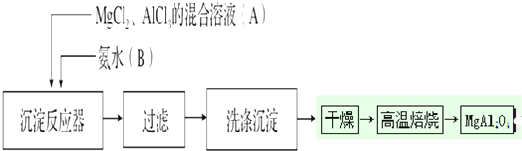
��1��д��AlCl3�백ˮ��Ӧ�Ļ�ѧ��Ӧ����ʽAlCl3+3NH3•H2O�TAl��OH��3��+3NH4Cl
��2���ж������г����Ƿ�ϴ�����õ��Լ��������ữ����������Һ�����±���ʱ������ʢ�Ź��������������������
��ˮAlCl3��183������������ʪ��������������������ʵ���ҿ�������װ���Ʊ���ͼ1��
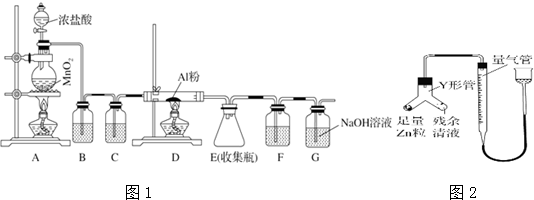
��3��������װ��A�����Ʊ�������д�������ӷ�Ӧ����ʽ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��
��װ��B��ʢ�ű���NaCl��Һ����װ�õ���Ҫ�����dz�ȥ���������е��Ȼ��⣮
��F���Լ���Ũ���ᣮ
��GΪβ������װ�ã����з�Ӧ�Ļ�ѧ����ʽ��Cl2+2NaOH�TNaCl+NaClO+H2O��
��4���Ʊ������ķ�Ӧ��������Ũ���½���ֹͣ��Ϊ�ⶨ��Ӧ����Һ�������Ũ�ȣ�̽��С��ͬѧ�������ʵ�鷽����
������������AgNO3��Һ��Ӧ���������ɵ�AgCl������
�ҷ�����������Zn��Ӧ���������ɵ�H2������̶����������жϺ�ʵ�飺
�ٳ����ж������������У��������������������������ᷴӦ��Ҳ����Ȼ��̷�Ӧ���ɳ�����
�ڽ����ҷ���ʵ�飺װ����ͼ2��ʾ���г���������ȥ����
��������Ӧ��ϣ�ÿ���1min��ȡ������������������μ�С��ֱ�����䣮���������μ�С��ԭ���ǿ�ʼʱ��Ӧ���ȣ������¶Ƚ��ͣ����������С���ų�������ʵ�������Ӱ�����أ���
��������ȡ������Һ10mL��������п����Ӧ����������Ͳ���ռ������������㵽�����Ϊ336mL����˵���������Ũ��С��3mol/Lʱ������������̷�Ӧ��
���� ��1��AlCl3��NH3•H2O��ӦAl��OH��3������NH4Cl��
��2�������������������ӣ��������������ữ�����������飻���չ���ҩƷ��������������
��3��Aװ��������ȡ������Ũ������лӷ��ԣ����ɵ������к���HCl��HCl��������ˮ������ʳ��ˮ�����������ܽ⣬����B��ʢ�ű���ʳ��ˮ����HCl����ˮAlCl3��183������������ʪ�����������������������������ں�Al��ӦǰӦ�ø����Cװ�����ڸ���������ΪŨ���Eװ�����ռ��Ȼ�����Gװ���������ն����������Fװ����������ˮ��������ֹ�Ȼ���ˮ�⣻
�ټ��������£�MnO2��Ũ���ᷴӦ����Cl2���Ȼ��̺�ˮ��
��Ũ������лӷ��ԣ����ɵ������к����Ȼ��⣬HCl��������ˮ������ʳ��ˮ���������ܽ⣻��
��Ũ���������ˮ�ԣ������������
��������NaOH��Һ��Ӧ�����Ȼ��ơ��������ƺ�ˮ��
��4������������HCl���Ȼ��̶���Ӧ����AgCl��ɫ������
�ڣ�������Ӧ��Ϻ����������С��������������ˮ��˵������������¶�Ӱ�죻
������n��H2��=$\frac{0.336L}{22.4L/mol}$=0.015mol������Hԭ���غ��n��HCl��=2n��H2��=2��0.015mol=0.03mol������C=$\frac{n}{V}$��������Ũ�ȣ�
��� �⣺��1��AlCl3��NH3•H2O��ӦAl��OH��3������NH4Cl����Ӧ����ʽΪAlCl3+3NH3•H2O�TAl��OH��3��+3NH4Cl���ʴ�Ϊ��AlCl3+3NH3•H2O�TAl��OH��3��+3NH4Cl��
��2�������������������ӣ��������������ữ�����������飬�����Ӻ������ữ����������Ӧ���ɰ�ɫ���������չ���ҩƷ��������������
�ʴ�Ϊ�������ữ����������Һ��������
��3��Aװ��������ȡ������Ũ������лӷ��ԣ����ɵ������к���HCl��HCl��������ˮ������ʳ��ˮ�����������ܽ⣬����B��ʢ�ű���ʳ��ˮ����HCl����ˮAlCl3��183������������ʪ�����������������������������ں�Al��ӦǰӦ�ø����Cװ�����ڸ���������ΪŨ���Eװ�����ռ��Ȼ�����Gװ���������ն����������Fװ����������ˮ��������ֹ�Ȼ���ˮ�⣻
�ټ��������£�MnO2��Ũ���ᷴӦ����Cl2���Ȼ��̺�ˮ�����ӷ���ʽΪMnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O���ʴ�Ϊ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��
��Ũ������лӷ��ԣ����ɵ������к����Ȼ��⣬HCl��������ˮ������ʳ��ˮ�к��������Ӷ����������ܽ⣬����B�������dz�ȥHCl���ʴ�Ϊ����ȥ���������е��Ȼ��⣻��
��Ũ���������ˮ�ԣ������������Fװ��������ˮ��������ֹG��ˮ��������E��ȷ���Է�ֹ�Ȼ���ˮ�⣬F��ʢ������ΪŨ���ᣬ�ʴ�Ϊ��Ũ���
�������ж�����ֱ���ſգ�������NaOH��Һ��Ӧ�����κ�ˮ����Ӧ����ʽΪCl2+2NaOH�TNaCl+NaClO+H2O���ʴ�Ϊ��Cl2+2NaOH�TNaCl+NaClO+H2O��
��4������������HCl���Ȼ��̶���Ӧ����AgCl��ɫ���������Բ��ܸ���AgCl������������������ʴ�Ϊ���������������������ᷴӦ��Ҳ����Ȼ��̷�Ӧ���ɳ�����
�ڣ�������Ӧ��Ϻ����������С��������������ˮ��˵������������¶�Ӱ�죬�����п�ķ�Ӧ�Ƿ��ȷ�Ӧ����Ӧ��Ϻ���Һ�¶Ƚ��ͣ��������������С���ʴ�Ϊ����ʼʱ��Ӧ���ȣ������¶Ƚ��ͣ����������С��
������n��H2��=$\frac{0.336L}{22.4L/mol}$=0.015mol������Hԭ���غ��n��HCl��=2n��H2��=2��0.015mol=0.03mol��C=$\frac{n}{V}$=$\frac{0.03mol}{0.01L}$=3 mol/L���ʴ�Ϊ��3mol/L��
���� ���⿼�������Ʊ�ʵ�鷽����ƣ�Ϊ��Ƶ���㣬�漰���ʵ������йؼ��㡢�����Ʊ��������Ʊ������ӷ�Ӧ��֪ʶ�㣬��ȷʵ��ԭ�������������ǽⱾ��ؼ���֪��ͼ1�и���װ�õ����ã��״����ǣ�4�����⣮

| A�� | ������ֵ�ߣ���ȼ�ղ�����ˮ����һ����������ȼ�� | |
| B�� | ����̫���ܵ������Դ���滯ʯȼ�ϣ������ڽ�Լ��Դ���������� | |
| C�� | ú������������һ���̶���ʵ����ú�ĸ�Ч��������� | |
| D�� | ʯ����Ϊ��Ҫ�Ŀ�������ԴӦ�ñ����������� |
| ��ʼ������pH | ��ȫ������pH | |
| Fe��OH��2 | 7.0 | 9.0 |
| Fe��OH��3 | 1.9 | 3.2 |
| Cr��OH��3 | 6.0 | 8.0 |
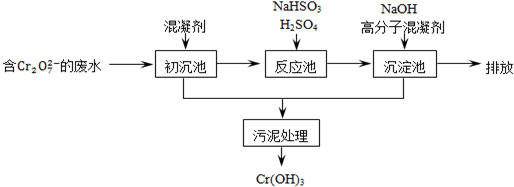
��1��Cr�����ڱ��е�λ��Ϊ�������ڵڢ�B�壮
��2���������м����������������������õ�ԭ���ǣ������ӷ���ʽ��ʾ��
Al3++3H2O?Al��OH��3+3H+��
��3���벹�䲢��ƽ���·�Ӧ���з�����Ҫ��Ӧ�����ӷ���ʽ��
1Cr2O72-+3HSO3-+5H+=2Cr3++3SO42-+4H2O��
��4�����ݡ����������͡��кͷ�����ԭ������������м���NaOH��Һ���˹����з�����Ҫ��Ӧ�����ӷ���ʽ�ǣ�H++OH-=H2O��Cr3++3OH-=Cr��OH��3����֤��Cr3+������ȫ�ķ�����ȡ��������ϲ���Һ�ⶨ��pH����pH��8���������ȫ��
| Ԫ�ش��� | �� | �� | �� | �� | �� | �� | �� | �� |
| ԭ�Ӱ뾶��nm�� | 0.186 | 0.160 | 0.037 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| ��Ҫ���ϼ� | +1 | +2 | +1 | +3 | +5��-3 | +7��-1 | +5��-3 | -2 |
��1���ٺ͢����γ�ԭ�Ӹ�����1��1��2��1�Ļ����ԭ�Ӹ�����Ϊ1��1�Ļ������д��ڵĻ�ѧ�������Ӽ��ͷǼ��Թ��ۼ���
��2��д����2���ߵ�ԭ�Ӻ�4���۵�ԭ�ӹ��ɵ����ʵĵ���ʽ��

��3��д���ܵ�����������Ӧˮ������ٵ�����������Ӧˮ�����ˮ��Һ��Ӧ�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O��
��4������������ȷ����ABCD������ĸ����
A���ۡ��ܴ��ڲ�ͬ����
B���ڵ����������������ӵĺ�����������
C������ͬ����Ԫ���зǽ�������ǿ
D����Ԫ�����Ԫ�����ߺ˵����֮����8
��5���١��ޡ�������γɶ����Σ�����һ�����Т١��ޡ�������Ԫ�ص�ԭ�Ӹ�����Ϊ1��1��1�����ε�����Ϊ�������ƣ�����ˮ��Һ����⻯���ˮ��Һ��Ӧ�����ɢĵ��ʣ��÷�Ӧ�����ӷ���ʽΪClO-+2H++Cl-�TCl2��+H2O��
| A�� | ������ˮ | B�� | ˮ��Һ�ܵ��� | C�� | ����״̬�ɵ��� | D�� | �۵�350�� |
 ���к͵ζ����ⶨ�ռ�Ĵ��ȣ����ռ��к��������Ӧ�����ʣ��Ը���ʵ��ش�
���к͵ζ����ⶨ�ռ�Ĵ��ȣ����ռ��к��������Ӧ�����ʣ��Ը���ʵ��ش�

