题目内容
【题目】如图分别表示红磷、白磷燃烧时的能量变化,有关说法正确的是( )
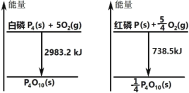
A.白磷比红磷稳定
B.白磷燃烧产物比红磷燃烧产物稳定
C.1mol 白磷转变为红磷放出 2244.7kJ 的热量
D.红磷燃烧的热化学方程式:4P(s)+5O2(g)→P4O10(s)+2954kJ
【答案】D
【解析】
从图中可以采集以下信息:P4(s)(白磷)+5O2(g)→P4O10(s)+2983.2kJ,P(s)(红磷)+![]() O2(g)→
O2(g)→![]() P4O10(s)+738.5kJ。
P4O10(s)+738.5kJ。
A.P4(s)(白磷)+5O2(g)→P4O10(s)+2983.2kJ,则![]() P4(s)(白磷)+
P4(s)(白磷)+![]() O2(g)→
O2(g)→![]() P4O10(s)+745.8kJ,相同质量的白磷燃烧放热多,则红磷比白磷稳定,A错误;
P4O10(s)+745.8kJ,相同质量的白磷燃烧放热多,则红磷比白磷稳定,A错误;
B.白磷和红磷的燃烧产物都为P4O10(s),产物的稳定性相同,B错误;
C.利用盖斯定律,可得P4(s)(白磷) →4P(s)(红磷)+29.2kJ,C错误;
D.红磷燃烧的热化学方程式:P(s)(红磷)+![]() O2(g)→
O2(g)→![]() P4O10(s)+738.5kJ ,则4P(s)+5O2(g)→P4O10(s)+2954kJ,D正确;
P4O10(s)+738.5kJ ,则4P(s)+5O2(g)→P4O10(s)+2954kJ,D正确;
故选D。

练习册系列答案
相关题目