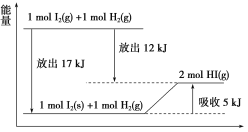
题目内容
【题目】将氯气持续通入紫色石蕊试液中,溶液颜色呈现如下变化:
![]()
关于溶液中导致变色的微粒Ⅰ、Ⅱ、Ⅲ的判断正确的是( )
A.H+、ClO-、Cl2B.H+、ClO-、Cl-C.HCl、ClO-、Cl-D.H+、HClO、Cl2
【答案】D
【解析】
由图中颜色变化可知,紫色石蕊试液中通入氯气,溶液变红色,表明溶液表现出酸性;溶液变为无色,表明溶液表现出强氧化性;溶液变为浅黄绿色,表明溶液中溶解了有色的物质。
氯气与水反应生成HCl、HClO,HCl具有酸性,HClO具有漂白性,则将氯气持续通入紫色石蕊试液中先变红后褪色,最后形成饱和氯水溶液显浅黄绿色为溶解的氯气分子,关于溶液中导致变色的微粒Ⅰ、Ⅱ、Ⅲ的判断正确的是D;
故选:D。

【题目】无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡与Cl2反应制备SnCl4。拟利用图中的仪器,设计组装一套实验装置制备SnCl4(每个装置最多使用一次)。
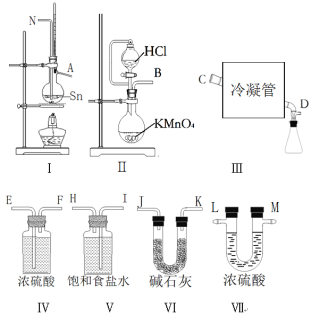
已知:①有关物理性质如下表
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ | |
Sn | 银白色固体 | 231.9 | 2260 | SnCl2易水解,SnCl4易水解生成固态二氧化锡, 锡与Cl2反应过程放出大量的热 |
SnCl4 | 无色液体 | -33 | 114 | |
SnCl2 | 无色晶体 | 246 | 652 |
②Fe3++Sn2+—Fe2++Sn4+ Fe2+ + Cr2O72- +H+—Fe3++Cr3++H2O(未配平)
回答下列问题:
(1)“冷凝管”的名称是________,装置Ⅱ中发生反应的离子方程式为________。
(2)用玻管(未画出)连接上述装置,正确的顺序是(填各接口的代码字母)_____。
(3)如何检验装置的气密性______,实验开始时的操作为_______。
(4)如果将制取的四氯化锡少许暴露于空气中,预期可看到的现象是出现白色烟雾,化学方程式为_______。
(5)可用重铬酸钾滴定法测定产品中的SnCl2的含量,准确称取该样品m g放于烧杯中,用少量浓盐酸溶解,加入过量的氯化铁溶液,再加水稀释,配制成250mL溶液,取25.00mL于锥形瓶中,用0.1000mol·L-1重铬酸钾标准溶液滴定至终点,消耗标准液15.00mL,则产品中SnCl2的含量为____%(用含m的代数式表示),在测定过程中,测定结果随时间延长逐渐变小的原因是____(用离子方程式表示)。