题目内容
6.已知A是气态烃,其相对分子量小于30.在如图所示的变化中,中间产物C跟葡萄糖一样也能跟新制的Cu(OH)2发生反应产生砖红色沉淀,E有香味,F是常见的一次性塑料包装袋的主要成分(反应条件未写出).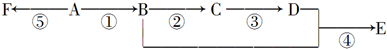
请回答下列问题:
(1)由A生成B的反应类型是加成反应,B生成C的反应类型是氧化反应.
(2)F的最简式为
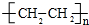 .
.(3)一次性塑料包装袋给我们生活带来便利的同时也带来了“白色污染”. 最近我国科学院以麦芽为原料,研制出的一种新型高分子可降解塑料--聚丁内酯(其结构:
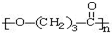 ),它可代替F,以减少“白色污染”. 聚丁内酯可用环丁内酯开环聚合而成,其工业生产方法和降解原理如下:
),它可代替F,以减少“白色污染”. 聚丁内酯可用环丁内酯开环聚合而成,其工业生产方法和降解原理如下: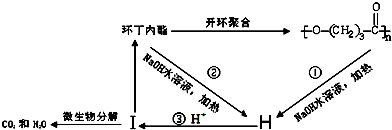
①写出环丁内酯的结构简式:
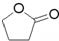 .
.②写出图中①的相应化学方程式
 .
.③写出I被微生物分解的化学方程式:2
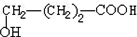 +9O2$\stackrel{微生物}{→}$8CO2↑+8H2O.
+9O2$\stackrel{微生物}{→}$8CO2↑+8H2O.
分析 (1)(2)A是气态烃,完全燃烧时产生的CO2和H2O的物质的量之比为1:1,最简式为CH2,A的相对分子量小于30,则A为CH2=CH2,在如图变化中,中间产物C跟葡萄糖一样也能跟新制的Cu(OH)2发生反应产生砖红色沉淀,E有香味,则C含有醛基、E属于酯,故乙烯与水发生加成反应生成B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,C进一步发生氧化反应生成D为CH3COOH,乙醇与乙酸发生酯化反应生成E为CH3COOC2H5,F是常见的一次性塑料包装袋的主要成分,则乙烯发生加聚反应生成F为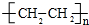 ;
;
(3)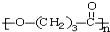 在氢氧化钠溶液中发生水解生成H,反应方程式为:
在氢氧化钠溶液中发生水解生成H,反应方程式为: ;环丁内酯通过开环聚合生成
;环丁内酯通过开环聚合生成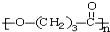 ,则环丁内酯的结构简式为
,则环丁内酯的结构简式为 ;H结果酸化生成I,则I的结构简式为:
;H结果酸化生成I,则I的结构简式为: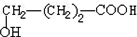 ,据此进行解答.
,据此进行解答.
解答 解:A是气态烃,完全燃烧时产生的CO2和H2O的物质的量之比为1:1,最简式为CH2,A的相对分子量小于30,则A为CH2=CH2,在如图变化中,中间产物C跟葡萄糖一样也能跟新制的Cu(OH)2发生反应产生砖红色沉淀,E有香味,则C含有醛基、E属于酯,故乙烯与水发生加成反应生成B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,C进一步发生氧化反应生成D为CH3COOH,乙醇与乙酸发生酯化反应生成E为CH3COOC2H5,F是常见的一次性塑料包装袋的主要成分,则乙烯发生加聚反应生成F为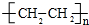 .
.
(1)由A生成B的反应类型是:加成反应,B生成C的反应类型是:氧化反应,
故答案为:加成反应;氧化反应;
(2)F的最简式为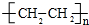 ,故答案为:
,故答案为: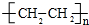 ;
;
(3)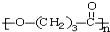 在氢氧化钠溶液中发生水解生成H:
在氢氧化钠溶液中发生水解生成H: ;环丁内酯通过开环聚合生成
;环丁内酯通过开环聚合生成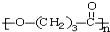 ,则环丁内酯的结构简式为
,则环丁内酯的结构简式为 ;H结果酸化生成I,则I的结构简式为:
;H结果酸化生成I,则I的结构简式为: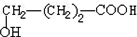 ,
,
①根据分析可知,环丁内酯的结构简式为: ,故答案为:
,故答案为: ;
;
②图中①的相应化学方程式: ,
,
故答案为: ;
;
③I被微生物分解的化学方程式:2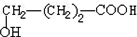 +9O2$\stackrel{微生物}{→}$8CO2↑+8H2O,
+9O2$\stackrel{微生物}{→}$8CO2↑+8H2O,
故答案为:2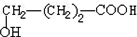 +9O2$\stackrel{微生物}{→}$8CO2↑+8H2O.
+9O2$\stackrel{微生物}{→}$8CO2↑+8H2O.
点评 本题考查有机物推断,属于拼合型题目,需要熟练掌握常见有机物结构与性质,成分利用题中信息、结构进行推断,试题侧重考查学生的分析理解能力、知识迁移能力,难度中等.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
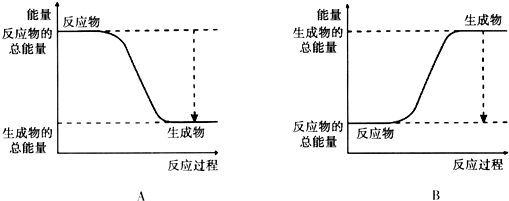
综合自测系列答案(1)已知该反应为放热反应,下图能正确表示该反应中能量变化的是A.
(2)从断键和成键的角度分析上述反应中能量的变化.已知:化学键的键能:
| 化学键 | H-H | O=O | H-O |
| 键能kJ•mol-1 | 436 | 496 | 463 |
(3)已知1克氢气完全燃烧生成液态水放出QKJ的热量,则氢气燃烧生成液态水的热化学反应方程式为2H2 (g)+O2(g)=2H2O(l)△H=-4QKJ/mol
(4)氢氧燃料电池的总反应方程式为2H2+O2═2H2O.电路中每转移0.2mol电子,标准状况下消耗H2的体积是2.24L.
| A. | 加热蒸干MgCl2饱和溶液,可制得氯化镁固体 | |
| B. | 明矾可用于水的消毒、杀菌 | |
| C. | 使用无磷洗衣粉,可缓解水体富营养化问题 | |
| D. | 用加热法可除去硬水中的CaCl2、MgCl2 |
| A. | 常温常压下,2.24L 氯气与氢氧化钠溶液完全反应转移的电子数为0.1NA | |
| B. | 标准状况下,1L辛烷完全燃烧后,所生成气体产物的分子数为8NA/22.4 | |
| C. | 0.1L 2mol•L-1的(NH4)2S溶液中含有的S2-数目为0.2 NA | |
| D. | 在含有4mol Si-O键的石英晶体中,氧原子的数目为2NA |
| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ②③ |
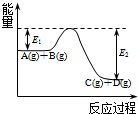 (1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).丙烷脱氢可得丙烯.
(1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).丙烷脱氢可得丙烯.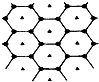 碳的一种单质石墨呈层状结构,有一碳镁新型材料就是在石墨碳原子层间加入镁原子层,两层俯视图:该材料的化学式为MgC2.
碳的一种单质石墨呈层状结构,有一碳镁新型材料就是在石墨碳原子层间加入镁原子层,两层俯视图:该材料的化学式为MgC2.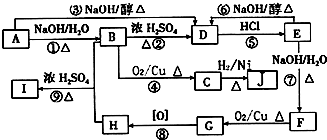
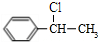 C中含氧官能团的名称为羰基.
C中含氧官能团的名称为羰基.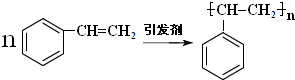 .G与新制Cu(OH)2悬浊液反应的化学方程式
.G与新制Cu(OH)2悬浊液反应的化学方程式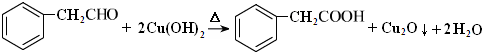 .
.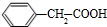 +
+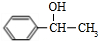 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$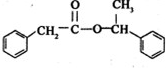 +H2O
+H2O