题目内容
19.某次酸雨的分析数据如下[NH4+]=2.0×10-5mol/L,[Cl-]=6.0×10-5mol/L,[Na+]=1.9×10-5mol/L,
[NO3-]=2.3×10-5mol/L,[SO42-]=2.8×10-5mol/L,
其他微粒离子忽略不计,计算该雨水的pH为4.
分析 根据溶液中电荷守恒计算酸雨中氢离子浓度,再根据pH的计算公式计算溶液的pH.
解答 解:溶液中阴阳离子所带电荷相等,设氢离子浓度为C,所以c (NH4+)+c (Na+)+C(H+)=c (NO3-)+2×c (SO42-)+c(Cl-),2×10-5mol/L+1.9×10-5mol/L+C(H+)=2.3×10-5mol/L+2×2.8×10-5mol/L+6×10-5mol/L,所以C(H+)=10-4 mol/L,pH=-lgC(H+)=4,
故答案为:4.
点评 本题考查了溶液的pH的简单计算,明确溶液中阴阳离子所带电荷相等是解本题的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.高温下,炽热的铁与水蒸气在密闭容器中进行反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g),下列条件的改变对其反应速率几乎无影响的是( )
| A. | 增加H2的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 压强不变,充入氮气使容器体积增大 | |
| D. | 体积不变,充入氮气使容器压强增大 |
4.据报道,一种“月球制氧机”可利用聚焦太阳能产生的高温加热月球土壤,制得氧气.据此可推测月球土壤中一定含有( )
| A. | 氧化物 | B. | 氧气 | C. | 水 | D. | 氧元素 |
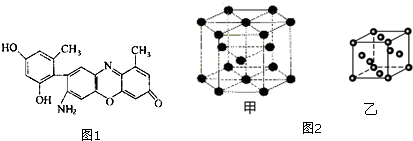


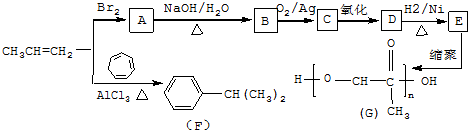
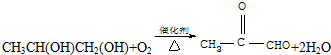 ,C发生银镜反应的化学方程式
,C发生银镜反应的化学方程式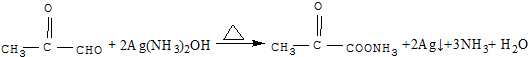 .
.