��Ŀ����
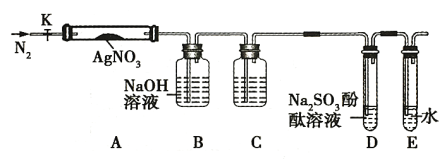
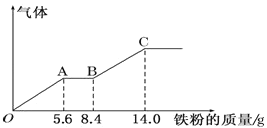
����Ŀ��ijϡ�����ϡ����Ļ����Һ 200mL��ƽ���ֳ����ݡ�������һ��������ͭ�ۣ�������ܽ�9.6 g������һ�����������ۣ�������������������������ӵı仯����ͼ��ʾ����֪����ֻ����ԭ Ϊ NO ���壩�����з�������������ǣ� ��
A.�ڶ�����Һ����������ΪFeSO4
B.OA �β������� NO��AB �εķ�ӦΪ Fe+2Fe3+�T3Fe2+��BC �β�������
C.ԭ�������HNO3 �����ʵ���Ϊ 0.8mol
D.H2SO4 Ũ��Ϊ 2.5molL-1
���𰸡�C
��������
������ϡ���ᷢ��������ԭ��Ӧ��������������ϡ���ᷴӦ�����ͼ�������������Ϊ�����������OA�η�����Ӧ��Fe+NO3-+4H+===Fe3++NO��+2H2O��AB�η�ӦΪ��Fe+2Fe3+===3Fe2+��BC�η�ӦΪ��Fe+2H+===Fe2++H2����
A��������������������ȫ������ԭ����Һ��û������������������Ƕ����������Եڶ�����Һ����������ΪFeSO4��Aѡ����ȷ��
B��OA�η�����Ӧ��Fe+NO3-+4H+===Fe3++NO��+2H2O��AB�η�ӦΪ��Fe+2Fe3+===3Fe2+��BC�η�ӦΪ��Fe+2H+===Fe2++H2����Bѡ����ȷ��
C��OA���������ȫ���������ã�Fe �� NO3-�����![]() ������ԭ�����Һ��
������ԭ�����Һ��![]() ����HNO3ҲΪ0.2mol��Cѡ�����
����HNO3ҲΪ0.2mol��Cѡ�����
D��������е����������������У�����������غ㣬����![]() ������H2SO4��Ũ��Ϊ
������H2SO4��Ũ��Ϊ![]() ��Dѡ����ȷ��
��Dѡ����ȷ��
��ѡC��

 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�����Ŀ��
��.�����£�����c(H+) ��ͬ�Ĵ���������ң�
(1)��ͬ�����£�ȡ������ļ�������Һ����ϡ��100����ϡ�ͺ����Һ����c(H+) ��С��ϵΪ��
�� _____________�� (������������С������������������ͬ)��
(2)��ȡ25 mL�ļ�������Һ���ֱ����Ũ�ȵ�NaOHϡ��Һ��ȫ��Ӧ�������ĵ�NaOH��Һ�������С��ϵΪV(��) _____________ V(��)��
��.��֪25 ��ʱ�й�����ĵ���ƽ�ⳣ�����£�
���ữѧʽ | HSCN | CH3COOH | HCN | H2CO3 |
����ƽ�ⳣ�� | 1.3��10-1 | 1.8��10-5 | 4.9��10-10 | Ka1=4.3��10-7 Ka2=5.6��10-11 |
(1)25 ��ʱ����20 mL 0.1 mol��L-1 CH3COOH��Һ��20 mL 0.1 mol��L-1 HSCN��Һ�ֱ���20 mL 0.1 mol��L-1 NaHCO3��Һ��ϣ�ʵ���ò������������(V)��ʱ��(t)�ı仯��ͼ��ʾ��
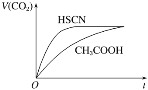
��Ӧ��ʼ��������Һ����CO2��������ʴ������Բ����ԭ���� _____________��
(2)�������¶Ȳ��䣬�ڴ�����Һ��ͨ��һ�������������и������С���� ______________(����ĸ)��
a.c(CH3COO-) b.c(H+) c.Kw d.�������ƽ�ⳣ��
III.(1)HClO4H2SO4HCl��HNO3����ǿ�ᣬ��������ˮ��Һ�в��������ij�¶������������ڱ������еĵ��볣��������˵������ȷ���� _________��
�� | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6��10-5 | Ka1��6.3��10-9 | 1.6��10-9 | 4.2��10-10 |
A.�¶Ȼ�Ӱ�����������ڱ����еĵ��볣��
B.�ڱ�������HClO4��������������ǿ����
C.�ڱ�������H2SO4�ĵ��뷽��ʽΪH2SO4===2H++SO42-
D.���������ڱ������ж�û����ȫ���룬��������ǿ�����
(2)�������Ƕ�Ԫ��ǿ�ᣬ25 ��ʱ������(H3PO3)�ĵ��볣��ΪK1=1��10-2K2=2.6��10-7��
���Դӵ���ƽ���ƶ��ĽǶȽ���K1Ϊʲô��K2��_______________________ ��
��д��������ĵ��뷽��ʽ(2��)_________________��_______________ ��
�������һ�ַ�����ʹ֮��ͨ��ֱ�۵�ʵ�������жϴ��������ǿ��H2S���÷������õ��Լ��� __________����Ӧ�Ļ�ѧ����ʽΪ _____________________��
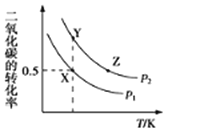
����Ŀ����һ�����İ����������ں��ݵ�������������У������������Բ�������ʹ��ﵽ��ѧƽ�⣺H2NCOONH4(s)![]() 2NH3(g)+CO2(g)��ʵ����ò�ͬ�¶��µ�ƽ�����������±�
2NH3(g)+CO2(g)��ʵ����ò�ͬ�¶��µ�ƽ�����������±�
�¶�/�� | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
ƽ����ѹǿ/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
ƽ��������Ũ��/10��3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
�����й�������ȷ����
A. �ڵ���������Ӧ����������
B. 15��ʱ������Ӧ�Ļ�ѧƽ�ⳣ��ԼΪ2.0
C. ���������ƽ������������������ʱ������Ӧ�ﵽ��ѧ��Ӧ��
D. ���������£���ԭƽ����ϵ���ٳ���2molNH3��1molCO2����ƽ���CO2Ũ�Ȳ���