题目内容
【题目】一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)Z(g),经1min达到平衡,剩余![]() 。下列说法正确的是
。下列说法正确的是
A.以Z浓度变化表示的反应速率为0.005mol/(Ls)
B.若增大压强,则物质Y的转化率减小
C.当c(X):c(Y):c(Z)=2:1:1时,表明反应处于平衡状态
D.若保持恒温恒压条件下再通入1molX和1molY进行反应,则平衡时X的转化率将不变
【答案】D
【解析】
经1min达到平衡,生成剩余![]() ,则
,则
![]() ,
,
开始(mol): 1 1 0
转化(mol): ![]()
![]()
![]()
平衡(mol): ![]()
![]()
![]()
A. 以Z浓度变化表示的反应速率为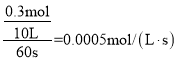 ,故A错误;
,故A错误;
B. 增大压强,平衡正向移动,则物质Y的转化率增大,故B错误;
C. 由以上计算可知当c(X):c(Y):c(Z)=4:7:3时,达到平衡状态,故C错误;
D. 若保持恒温恒压条件下再通入1molX和1molY进行反应,为等效平衡状态,则平衡时X的转化率将不变,故D正确;
答案选D。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
【题目】![]() 是一种新型硝化剂,在一定温度下可发生如下反应:
是一种新型硝化剂,在一定温度下可发生如下反应:![]() ,
,![]() 温度时,向密闭容器中通入
温度时,向密闭容器中通入![]() 气体,部分实验数据见下表:
气体,部分实验数据见下表:
时间 | 0 | 500 | 1000 | 1500 |
|
|
|
|
|
下列说法正确的是
A.500s内![]() 的生成速率为
的生成速率为![]()
B.![]() 温度下该反应平衡时
温度下该反应平衡时![]() 的转化率为
的转化率为![]()
C.达平衡后其他条件不变,将容器体积压缩到原来的![]() ,
,![]()
D.![]() 温度下的平衡常数为
温度下的平衡常数为![]() ,
,![]() 温度下的平衡常数为
温度下的平衡常数为![]() ,若
,若![]() ,则
,则![]()