题目内容
11.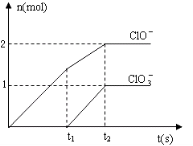 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.(1)t2时,Ca(OH)2与Cl2发生反应的总的化学方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O.
(2)该石灰乳中含有Ca(OH)2的物质的量是5 mol.
分析 由图可知,t2时n(C1O-)=2mol,n(C1O3-)=1mol,氯气与氢氧化钙反应生成CaCl2、Ca(ClO)2、Ca(ClO3)2、H2O,且n[Ca(ClO)2]:n[Ca(ClO3)2]=2:1,反应方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O,结合反应计算石灰乳中含有Ca(OH)2的物质的量.
解答 解:(1)由图可知,t2时n(C1O-)=2mol,n(C1O3-)=1mol,氯气与氢氧化钙反应生成CaCl2、Ca(ClO)2、Ca(ClO3)2、H2O,且n[Ca(ClO)2]:n[Ca(ClO3)2]=2:1,反应方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O,
故答案为:10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O;
(2)由图可知,t2时氢氧化钙与氯气恰好反应,n(C1O-)=2mol,故n[Ca(ClO)2]=1mol,n(C1O3-)=1mol,故n[Ca(ClO3)2]=0.5mol,根据方程式10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O可知,n[Ca(OH)2]=10n[Ca(ClO3)2]=0.5mol×10=5mol,
故答案为:5.
点评 本题考查氧化还原反应的计算,为高频考点,把握反应与图象的对应关系为解答的关键,注意电子守恒及反应的书写,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
1.取一定质量的某物质在ag氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后容器内有bg氧气,测得b>a.下列物质中满足上述结果的是( )
| A. | HCOOH | B. | HCHO | C. | CH4 | D. | C6H12O6 |
2.核磁共振氢谱是测定有机分子结构最有用的工具之一.在有机物分子中,不同的氢原子在核磁共振氢谱中给出的峰值(信号)不同.根据峰值(信号)可以确定有机物中氢原子的种类.下列有机物分子中,在核磁共振氢谱中只给出一种峰(信号)的是( )
| A. | CH30H | B. | CH3COCH3 | C. | CH3COOH | D. | CH3COOCH3 |
6.如表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答问题:
(1)表中所注A-I元素,(填元素符号或化学式)化学性质最不活泼的元素是Ne,只有负价而无正价的是F,氧化性最强的单质是F2,还原性最强的单质是Na;
(2)表中所注A-I元素,其中H元素的最高化合价是+7;形成化合物种类最多的元素是C;
(3)D可与O元素形成两种化合物分别是CO、CO2
(4)在B、C、D、E、F、G、H中,原子半径最大的是Na
(5)A和E形成化合物的化学式NH3等.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)表中所注A-I元素,其中H元素的最高化合价是+7;形成化合物种类最多的元素是C;
(3)D可与O元素形成两种化合物分别是CO、CO2
(4)在B、C、D、E、F、G、H中,原子半径最大的是Na
(5)A和E形成化合物的化学式NH3等.
16.某烃分子中有一个由C-C键构成的六元环,有一个C=C键,还有一个C≡C键,则能满足上述烃的分子式可能是( )
| A. | C8H10 | B. | C10H16 | C. | C12H22 | D. | C14H22 |
3.下列物质中属于纯净物的是( )
①由同种元素组成的物质
②具有固定熔沸点的物质
③由相同种类和相同数目的原子组成的分子
④只有一种元素的阳离子和另一种元素的阴离子组成的物质
⑤在氧气中燃烧只生成二氧化碳的物质
⑥只含有一种分子的物质.
①由同种元素组成的物质
②具有固定熔沸点的物质
③由相同种类和相同数目的原子组成的分子
④只有一种元素的阳离子和另一种元素的阴离子组成的物质
⑤在氧气中燃烧只生成二氧化碳的物质
⑥只含有一种分子的物质.
| A. | 仅②③⑥ | B. | 仅④⑤⑥ | C. | 仅①④ | D. | 仅②⑥ |
20.一些烷烃的燃烧热数值(kJ•mol-1)如表:下列推断正确的是( )
| 化合物 | 甲烷 | 乙烷 | 丙烷 | 正丁烷 | 异丁烷 | 异戊烷 |
| 燃烧热 (kJ•mol-1) | 891.0 | 1560.8 | 2221.5 | 2878.0 | 2869.6 | 3531.3 |
| A. | 正丁烷?异丁烷△H<0 | |
| B. | 乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)═CO2(g)+6H2O(g)△H=-1560.8 kJ•mol-1 | |
| C. | 正戊烷的燃烧热数值小于3531.3 kJ•mol-1 | |
| D. | 相同质量的烷烃,随碳原子数增加,燃烧放出的热量增多 |
1.升高温度,下列常数中不一定增大的是( )
| A. | 平衡常数K | B. | 电离常数Ka | ||
| C. | 水的离子积常数Kw | D. | 盐的水解常数Kh |