题目内容
3.下列物质中属于纯净物的是( )①由同种元素组成的物质
②具有固定熔沸点的物质
③由相同种类和相同数目的原子组成的分子
④只有一种元素的阳离子和另一种元素的阴离子组成的物质
⑤在氧气中燃烧只生成二氧化碳的物质
⑥只含有一种分子的物质.
| A. | 仅②③⑥ | B. | 仅④⑤⑥ | C. | 仅①④ | D. | 仅②⑥ |
分析 单质是只有一种元素组成的纯净物,化合物是至少两种元素组成的纯净物,据此解答.
解答 解:①由同种元素组成的物质可能是混合物,例如臭氧与氧气组成物质,故错误;
②只有纯净物才具有固定的熔沸点,故正确;
③同分异构体之间是由相同种类和相同数目的原子组成的分子,是混合物,例如乙醇与甲醚,故错误;
④钠和氧形成的化合物有2种,如氧化钠和过氧化钠组成的物质,属于混合物,故错误;
⑤碳元素存在多种同素异形体,金刚石、石墨、C60,燃烧产物都为二氧化碳,组成的物质属于混合物,故错误;
⑥同种微粒构成的是纯净物,故正确;
故选:D.
点评 本题考查纯净物和混合物的区别,明确概念的内涵是解题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.下表是A、B、C、D四种有机物的有关信息:
回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成物质E,与E在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体;②有毒;③不溶于水;④密度比水大;⑤与酸性KMnO4溶液和溴水反应褪色;⑥任何条件下不与氢气反应.写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$ +H2O.
+H2O.
(4)C与D反应能生成相对分子质量为100的酯,该反应的反应类型为酯化反应(取代反应);其化学方程式为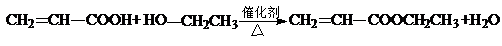 .
.
| A | 1使溴的四氯化碳溶液褪色;②比例模型为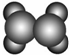 ;③能与水在一定条件下反应生成C ;③能与水在一定条件下反应生成C |
| B | 1C、H两种元素组成;②球棍模型为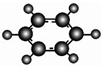 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与D反应生成相对分子质量为100的酯 |
| D | ①由C、H、O三种元素组成;②球棍模型为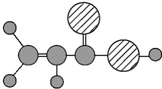 |
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成物质E,与E在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体;②有毒;③不溶于水;④密度比水大;⑤与酸性KMnO4溶液和溴水反应褪色;⑥任何条件下不与氢气反应.写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$ +H2O.
+H2O.(4)C与D反应能生成相对分子质量为100的酯,该反应的反应类型为酯化反应(取代反应);其化学方程式为
15.在化工生产和科学研究中各种酸具有重要的用途.
(1)磷酸是一种三元中强酸,在溶液中各种含P粒子的百分数(δ)与溶液的pH关系如图:则磷酸的第二级电离平衡常数约为10-7;Na2HPO4溶液的pH约为10,说明HPO4-水解程度大于电离程度(用其电离与水解程度来解释),Na2HPO4溶液的物料守恒式为c(Na+)=2[c(H3PO4)+c(H2PO4-)+c(HPO42-)+c(PO43-)].
(2)乙酸(用HAC来表示)是一种重要的化工原料也可作溶剂.HClO4、HCl、HNO3、H2SO4在无水乙酸中都是弱酸,存在如下电离平衡(电离常数均为常温下的数值):
HClO4+HAC═H2AC++ClO4-K═1.6×10-5
HCl+HAC═H2AC++Cl-K═1.6×10-9
HNO3+HAC═H2AC++NO3-K═4.2×10-10
H2SO4+HAC═H2AC++HSO4-K═6.3×10-9
①H2AC+的名称为乙酸合氢离子;用乙酸作溶剂时,HClO4、HCl、HNO3、H2SO4的酸性由强到弱的排序为HClO4、H2SO4、HCl、HNO3;在0.01mol/L HNO3的乙酸溶液中,c(NO3-)=2×10-6(计算结果保留一位有效数字).
②已知如表酸在水中的电离常数(25℃)
则在相同条件下0.1mol/L HClO4的乙酸溶液与0.1 mol/L HAc水溶液导电能力最接近.
(3)混酸(浓硫酸和浓硝酸的混合物)是常用的硝化试剂,其中含有硝化反应的中间体NO2+,其反应是:2H2SO4+HNO3═[NO2]+[HSO4]-+[H3O+][HSO4]-.根据中和反应的原理判断此反应中HNO3作为碱;NO2+与CO2或N2O或N3-或-OCN(填化学式)的原子数和电子数相同、结构相似;H3O+的空间构型为三角锥形.
(1)磷酸是一种三元中强酸,在溶液中各种含P粒子的百分数(δ)与溶液的pH关系如图:则磷酸的第二级电离平衡常数约为10-7;Na2HPO4溶液的pH约为10,说明HPO4-水解程度大于电离程度(用其电离与水解程度来解释),Na2HPO4溶液的物料守恒式为c(Na+)=2[c(H3PO4)+c(H2PO4-)+c(HPO42-)+c(PO43-)].
(2)乙酸(用HAC来表示)是一种重要的化工原料也可作溶剂.HClO4、HCl、HNO3、H2SO4在无水乙酸中都是弱酸,存在如下电离平衡(电离常数均为常温下的数值):
HClO4+HAC═H2AC++ClO4-K═1.6×10-5
HCl+HAC═H2AC++Cl-K═1.6×10-9
HNO3+HAC═H2AC++NO3-K═4.2×10-10
H2SO4+HAC═H2AC++HSO4-K═6.3×10-9
①H2AC+的名称为乙酸合氢离子;用乙酸作溶剂时,HClO4、HCl、HNO3、H2SO4的酸性由强到弱的排序为HClO4、H2SO4、HCl、HNO3;在0.01mol/L HNO3的乙酸溶液中,c(NO3-)=2×10-6(计算结果保留一位有效数字).
②已知如表酸在水中的电离常数(25℃)
| 酸 | HCN | HAc | HF | H2SO3 |
| Ka | 4.9×10-10 | 1.75×10-5 | 3.5×10-4 | K1=1.5×10-2 |
(3)混酸(浓硫酸和浓硝酸的混合物)是常用的硝化试剂,其中含有硝化反应的中间体NO2+,其反应是:2H2SO4+HNO3═[NO2]+[HSO4]-+[H3O+][HSO4]-.根据中和反应的原理判断此反应中HNO3作为碱;NO2+与CO2或N2O或N3-或-OCN(填化学式)的原子数和电子数相同、结构相似;H3O+的空间构型为三角锥形.

13.下列实验操作错误的是( )
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 滴定时,左手控制滴定管活塞,右手握持锥形瓶,眼睛注视滴定管中的液面 | |
| D. | 用精密pH试纸测得溶液的pH为4.2 |
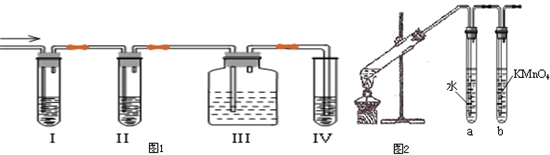
 实验室用如图装置制取少量溴苯,试填写下列空白.
实验室用如图装置制取少量溴苯,试填写下列空白.
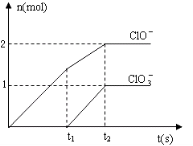 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.