题目内容
NA表示阿伏加德罗常数,有关NA的正确说法是( )
| A、1mol D318O+中含有的中子数为10NA |
| B、标准状况下,22.4L水中含O-H键数为2NA |
| C、某温度时1L pH=6的纯水所含OH-离子数为1.0×10-6NA |
| D、7.8g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.D318O+中含有13个中子,1molD318O+中含有13mol中子;
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.纯水中氢离子与氢氧根离子浓度相等;
D.过氧化钠与硫化钠的摩尔质量但是78g/mol,0.1mol硫化钠和过氧化钠中含有0.1mol阴离子.
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.纯水中氢离子与氢氧根离子浓度相等;
D.过氧化钠与硫化钠的摩尔质量但是78g/mol,0.1mol硫化钠和过氧化钠中含有0.1mol阴离子.
解答:
解:A.1molD318O+中含有13mol中子,含有的中子数为13NA,故A错误;
B.标况下水不是气体,不能使用标况下的摩尔体积计算22.4L水的物质的量,故B错误;
C.某温度时1L pH=6的纯水中,氢离子浓度为1.0×10-6mol/L,纯水中氢氧根离子与氢离子浓度相等,所以1L纯水中含有1.0×10-6mol氢氧根离子,所含OH-离子数为1.0×10-6NA,故C正确;
D.7.8g Na2S和Na2O2的物质的量为0.1mol,0.1mol硫化钠和过氧化钠的混合物中含有0.1mol阴离子,含有的阴离子数为0.1NA,故D错误;
故选C.
B.标况下水不是气体,不能使用标况下的摩尔体积计算22.4L水的物质的量,故B错误;
C.某温度时1L pH=6的纯水中,氢离子浓度为1.0×10-6mol/L,纯水中氢氧根离子与氢离子浓度相等,所以1L纯水中含有1.0×10-6mol氢氧根离子,所含OH-离子数为1.0×10-6NA,故C正确;
D.7.8g Na2S和Na2O2的物质的量为0.1mol,0.1mol硫化钠和过氧化钠的混合物中含有0.1mol阴离子,含有的阴离子数为0.1NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标准状况下水的状态不是气体,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项A为易错点,注意D318O+中含有13个中子.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列操作或发生事故时的处理方法正确的是( )
| A、可用燃着的酒精灯引燃另一只酒精灯 |
| B、给试管里的液体加热时,试管应与桌面垂直 |
| C、凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
| D、浓硫酸不慎沾在皮肤上,应立即用干布擦掉,然后用水冲洗,最后再涂上3%~5%的小苏打溶液 |
下列说法正确的是( )
| A、能白发进行的化学反应一定是△H<O、△S>O |
| B、已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ?mol-1,则含40.Og NaOH的稀溶液与稀醋酸完全中和,放出的热量小于57.3kJ |
| C、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1,则氢气的燃烧热为241.8kJ?mol-1 |
| D、已知2C(s)+2O2(g)═2CO2(g)△H=a kJ?mol-1、2C(s)+O2(g)═2CO(g)△H═b kJ?mol-1,则a>b |
下列表示对应化学反应的离子方程式正确的是( )
A、MnO2与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| B、醋酸溶解鸡蛋壳:2H++CaCO3=Ca2++CO2↑+H2O | ||||
| C、NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ | ||||
| D、向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
下列有关有机物同分异构体说法中不正确的是( )
| A、分子式为C4H8的同分异构体共有(不考虑立体异构)5种 |
| B、立方烷(C8H8)的六氯取代物有3种 |
| C、分子式为C5H12O的同分异构体中属于醇类的有7种 |
D、 的一溴取代物有4种 的一溴取代物有4种 |
NaNO2是一种食品添加剂,它能致癌.酸性KMnO4溶液与NaNO2的反应方程式是(未配平):MnO4-+NO2-+□→Mn2++NO3-+H2O.下列叙述中正确的是( )
| A、该反应中NO2-是还原剂 |
| B、反应过程中溶液的pH减小 |
| C、生成1mol NaNO3时消耗2.5mol KMnO4 |
| D、□中的粒子是OH- |
下列有关化学反应速率的说法中,正确的是( )
| A、100mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
| B、用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 |
| C、二氧化硫的催化氧化是一个放热反应,所以升高温度,反应速率减慢 |
| D、汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢 |
有关Na2CO3和NaHCO3的性质,下列叙述错误的是( )
| A、等质量的Na2CO3和NaHCO3与足量的盐酸反应,在相同条件下NaHCO3产生的CO2气体体积大 |
| B、同一温度下,与等浓度的盐酸反应时,NaHCO3比Na2CO3剧烈 |
| C、与同种酸反应生成等量的CO2时,所消耗的酸的量相等 |
| D、将石灰水加入到NaHCO3溶液中将会产生沉淀 |
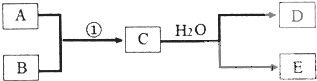 已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系:
已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系: