题目内容
煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ)
CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g) CaS(s) + 4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
CaS(s) + 4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)反应Ⅰ能自发进行的条件是 。
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅱ的Kp= (用表达式表示)。
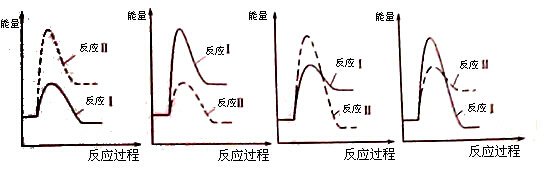
(3)假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是 。
(4)通过监测反应体系中气体浓度的变化判断反应Ⅰ和Ⅱ是否同时发生,理由是 。
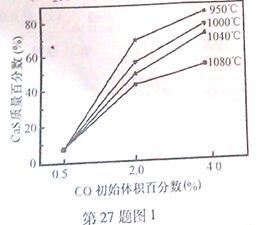
(5)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO2生成量的措施有 。
A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温度
C.提高CO的初始体积百分数
D.提高反应体系的温度
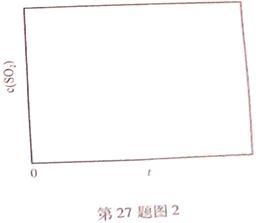
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2,请在图2中画出反应体系中c(SO2)随时间t变化的总趋势图。
CaSO4(s)+CO(g)
 CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ)
CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ) CaSO4(s)+4CO(g)
 CaS(s) + 4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
CaS(s) + 4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)请回答下列问题:
(1)反应Ⅰ能自发进行的条件是 。
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅱ的Kp= (用表达式表示)。
(3)假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是 。

(4)通过监测反应体系中气体浓度的变化判断反应Ⅰ和Ⅱ是否同时发生,理由是 。
(5)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO2生成量的措施有 。
A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温度
C.提高CO的初始体积百分数
D.提高反应体系的温度
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2,请在图2中画出反应体系中c(SO2)随时间t变化的总趋势图。


(1)高温
(2)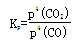
(3)C.
(4) 反应I中生成有SO2,监测SO2与CO2的浓度增加量的比不为1:1,可确定发生两个反应。
(5)A、B、C
(6)
(2)
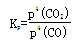
(3)C.
(4) 反应I中生成有SO2,监测SO2与CO2的浓度增加量的比不为1:1,可确定发生两个反应。
(5)A、B、C
(6)

试题分析:(1)由△G=△H-T△S<0时自发,△H>0,则T要大,故选择高温。
(3)反应Ⅰ吸热,产物的能量高于反应物,反应Ⅱ放热,产物的能量低于反应物;反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),反应I的活化能低。
(4) 反应I中生成有SO2,监测SO2与CO2的浓度增加量的比即可确定是否发生两个反应。
(5)向该反应体系中投入石灰石,产生CO2,使反应I逆向进行,可降低该反应体系中SO2生成量,A正确;在合适的温度区间内控制较低的反应温度,图中可以看出最低温度的CaS的含量最高,故B正确、D错误;C.图中可以看出,提高CO的初始体积百分数,可以提高CaS的含量,故正确。
(6) 反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),故SO2增加的快,反应达到平衡快;随着反应II的进行,CO2的浓度不断增大,使反应I平衡逆向移动。A为阿伏加德罗常数的值来表示微粒数目。

练习册系列答案
相关题目
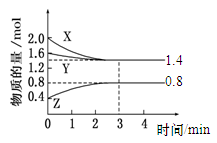
 2Z(g)
2Z(g) 2G(g)。有关数据如下:
2G(g)。有关数据如下: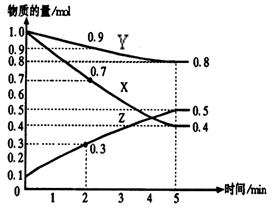
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g) 2SO3(g) △H=-196kJ/mol,提高反应中SO2的转化率,是减少SO2排放的有效措施。
2SO3(g) △H=-196kJ/mol,提高反应中SO2的转化率,是减少SO2排放的有效措施。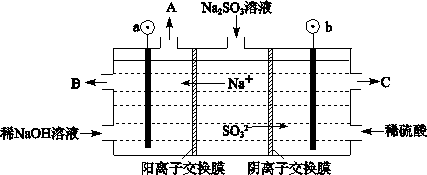
 2C来说,下列反应速率最快的是:( )
2C来说,下列反应速率最快的是:( )