题目内容
在一定条件下,将E(g)和F(g)充入体积不变的2 L密闭容器中,发生下述反应,并于5 min末达到平衡:2E(g)+F(g) 2G(g)。有关数据如下:
2G(g)。有关数据如下:
下列判断正确的是
A.反应在前5min内,v(E)=0.04 mol/(L·min)
B.其他条件不变,若增大E的浓度,则达平衡时E的转化率会增大
C.其他条件不变,降低温度,平衡时n(E)=3.0mol,则反应的△H>0
D.平衡后移走2.0 mol E和1.0 mol F,在相同条件下再达平衡时,c(G)<0.2 mol?L-1
 2G(g)。有关数据如下:
2G(g)。有关数据如下:| | E(g) | F(g) | G(g) |
| 初始浓度(mol?L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol?L-1) | c1 | c2 | 0.4 |
A.反应在前5min内,v(E)=0.04 mol/(L·min)
B.其他条件不变,若增大E的浓度,则达平衡时E的转化率会增大
C.其他条件不变,降低温度,平衡时n(E)=3.0mol,则反应的△H>0
D.平衡后移走2.0 mol E和1.0 mol F,在相同条件下再达平衡时,c(G)<0.2 mol?L-1
D
试题分析:A、反应在前5min内,根据题给数据图表分析,c1=1.6mol/L,c2=0.2mol/L,E的物质的量浓度变化为0.4 mol/L,反应速率v(E)=△c/△t=0.02mol/(L?min),错误;B、两种或两种以上物质反应,增大一种的浓度会提高另一种反应物的转化率,而本身转化率减小,其他条件不变,若增大E的浓度,则达平衡时E的转化率会减小,错误;C、降低温度,E物质的量减小,说明平衡正向进行,正反应为放热反应,△H<0,错误;D、起始量为E为4mol,F为2mol,平衡后移走2.0mol E和1.0mol F,相当于起始量减半,压强减小平衡逆向进行,G的浓度小于0.2mol/L,正确。

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
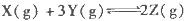 为放热反应,一定温度下在密闭容器中进行反应,
为放热反应,一定温度下在密闭容器中进行反应,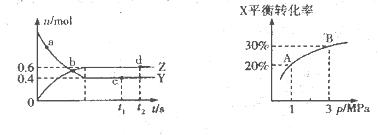
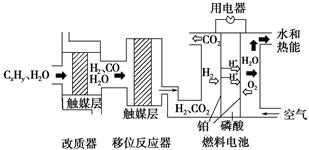
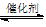 CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大
CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大 CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ)
CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ) 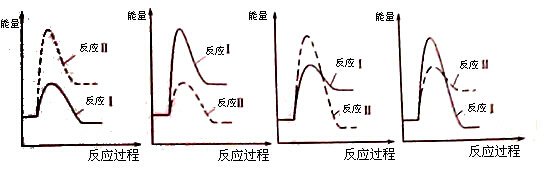
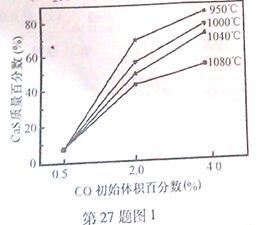
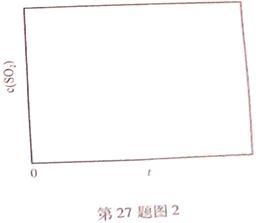
 CH3OH+H2O。请回答下列问题:
CH3OH+H2O。请回答下列问题: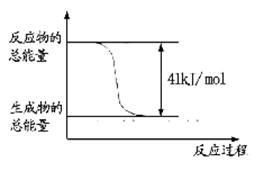
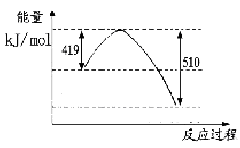 写出由二氧化碳和氢气制备甲醇的热化学方程式__ _。
写出由二氧化碳和氢气制备甲醇的热化学方程式__ _。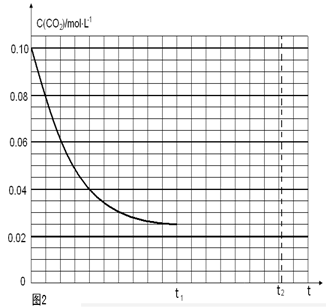
 4NO+6H2O,若在反应开始后5s~10s之间的反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列判断正确的关系是( )。
4NO+6H2O,若在反应开始后5s~10s之间的反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列判断正确的关系是( )。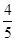 v(NH3)=v(O2)
v(NH3)=v(O2) 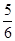 v(O2)=v(H2O)
v(O2)=v(H2O) v(NH3)=v(H2O)
v(NH3)=v(H2O)