题目内容
【题目】下列说法正确的是( )
A.CH4和C15H32为同系物
B.分子式为C4H8BrCl的有机物共有11种(不含立体异构)
C.化合物![]() (b)、
(b)、![]() (d)、正戊烷(p)中只有b的所有碳原子可能处于同一平面
(d)、正戊烷(p)中只有b的所有碳原子可能处于同一平面
D.CH3CH=CHCH3分子中的四个碳原子在同一直线上
【答案】A
【解析】
A.CH4和C15H32都属于烷烃,分子式不同,互为同系物,选项A正确;
B.C4H8BrCl可以看作C4H10中2个H原子被Cl、Br原子取代,而丁烷有CH3CH2CH2CH3、CH3CH(CH3)2两种,先分析碳骨架异构,分别为 C-C-C-C 与![]() 2种情况,然后分别对2 种碳骨架采用“定一移一”的方法分析,其中骨架 C-C-C-C 有
2种情况,然后分别对2 种碳骨架采用“定一移一”的方法分析,其中骨架 C-C-C-C 有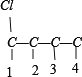 、
、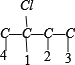 共 8 种,骨架
共 8 种,骨架![]() 有
有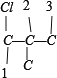 、
、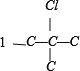 ,共 4 种,总共12种,选项B错误;
,共 4 种,总共12种,选项B错误;
C.![]() (d)、正戊烷(p)都含有饱和碳原子,具有甲烷的结构特点,则
(d)、正戊烷(p)都含有饱和碳原子,具有甲烷的结构特点,则![]() (d)、正戊烷(p)所有原子不可能处于同一平面,只有
(d)、正戊烷(p)所有原子不可能处于同一平面,只有![]() (b)为平面形结构,选项C错误;
(b)为平面形结构,选项C错误;
D.CH3CH=CHCH3分子中的四个碳原子和乙烯分子中4个氢原子两个碳原子结构相似为平面结构,四个碳原子不在同一直线上,选项D错误;
答案选A。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目