题目内容
【题目】在密闭容器中某气态烃和氧气按一定比例混和,燃烧后恢复到原温度(20℃),压强减小至原来的一半,若加NaOH溶液气体全部被吸收,则此烃可能为( )
A.C2H4B.C2H6C.C3H6D.CH4
【答案】A
【解析】
根据有机物燃烧的反应方程式,在限制条件下确定有机物的分子式。
压强之比等于物质的量之比,反应后容器压强为原来的一半,则反应后气体的物质的量是反应前的一半,按照烃燃烧的通式:![]() ,20℃时,水为液态,根据系数得
,20℃时,水为液态,根据系数得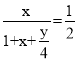 ,解得
,解得![]() ;
;
A.C2H4代入以上计算式,满足条件,A正确;
B.C2H6代入以上计算式,不满足条件,B错误;
C.C3H6代入以上计算式,不满足条件,C错误;
D.CH4代入以上计算式,不满足条件,D错误;
答案选A。

练习册系列答案
相关题目