题目内容
下列关于卤素单质的叙述,不正确的是( )
| A、单质的颜色随核电荷数的增加逐渐变深 |
| B、随核电荷数的增加单质的氧化性逐渐增强 |
| C、随核电荷数的增加气态氢化物的稳定性逐渐减弱 |
| D、单质的熔沸点随核电荷数的增加逐渐升高 |
考点:卤素原子结构及其性质的比较,氯、溴、碘及其化合物的综合应用
专题:元素周期律与元素周期表专题,卤族元素
分析:卤族元素由上到下,颜色加深、单质的沸点升高、非金属性增强、得电子能力增强,据此分析的.
解答:
解:A.卤族元素单质的颜色随着核电荷数增大而加深,颜色变化为:淡黄绿色→黄绿色→深红棕色→紫黑色,故A正确;
B.卤族元素非金属性从上到下逐渐减弱,则其单质的氧化性逐渐减弱,故B错误;
C.卤族元素非金属性从上到下逐渐减弱,所以其氢化物稳定性逐渐减弱,故C正确;
D.卤族元素单质的熔沸点与其相对分子质量成正比,从上到下其单质的相对分子质量增大,则其单质的沸点升高,故D正确;
故选B.
B.卤族元素非金属性从上到下逐渐减弱,则其单质的氧化性逐渐减弱,故B错误;
C.卤族元素非金属性从上到下逐渐减弱,所以其氢化物稳定性逐渐减弱,故C正确;
D.卤族元素单质的熔沸点与其相对分子质量成正比,从上到下其单质的相对分子质量增大,则其单质的沸点升高,故D正确;
故选B.
点评:本题考查了原子结构和性质的关系,明确同一主族元素周期律内涵即可解答,知道非金属性强弱的判断方法,注意分子晶体的熔沸点与其相对分子质量有关,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
除去CO2的SO2不能选用的试剂是( )
| A、NaOH溶液反应 |
| B、高锰酸钾溶液 |
| C、溴水 |
| D、饱和的 NaHCO3溶液 |
在稀CH3COOH溶液中存在如下电离平衡:CH3COOH═CH3COO-+H+,下列叙述正确的是( )
| A、加入水时,平衡左移 |
| B、加入少量0.1mol/L HCl溶液,溶液中c(H+)减小 |
| C、加入少量NaOH固体,平衡右移 |
| D、加入少量CH3COONa固体,平衡右移 |
设nA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、22.4L O3中含3nA个氧原子 |
| B、标准状况下,22.4L CH2Cl2含有2nA氯原子 |
| C、1mol SO2与足量的H2S充分反应,转移2nA个电子 |
| D、17g H2O2中含有9nA个质子 |
下列事实不能说明一元酸HA为弱酸的是( )
| A、常温下0.1mol?L-1的HA溶液pH为5 |
| B、常温下NaA溶液的pH>7 |
| C、HA溶液中存在H+、OH-、A-、HA |
| D、HA溶液能与大理石反应 |
如表代表周期表中的几种短周期元素,下列说法中正确的是( )
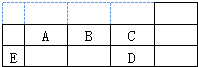

| A、C、D的氢化物沸点D比C高 |
| B、第一电离能A、B、C依此增大 |
| C、A、B、C中电负性最大的A |
| D、五种元素中,最高价氧化物对应的水化物酸性最强的是D |
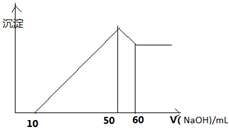 某溶液中含有H+、Al3+、Mg2+、Cu2+四种阳离子,且Mg2+ Cu2+物质的量之为1:1,逐滴加入0.1moL/L NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+、Cu2+四种阳离子的物质的量浓度之比为( )
某溶液中含有H+、Al3+、Mg2+、Cu2+四种阳离子,且Mg2+ Cu2+物质的量之为1:1,逐滴加入0.1moL/L NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+、Cu2+四种阳离子的物质的量浓度之比为( )| A、1:1:1:1 |
| B、2:2:1:1 |
| C、2:1:1:1 |
| D、4:4:1:1 |
pH相等的氨水和氢氧化钠溶液,分别用蒸馏水稀释相同倍数后,两溶液pH的关系是( )
| A、前者大 | B、后者大 |
| C、相等 | D、无法比较 |
Fe与HNO3反应随温度和HNO3的浓度不同而产物不同.已知0.2mol HNO3作氧化剂时,恰好把0.2mol Fe氧化,则HNO3可能被还原成( )
| A、NH4+ |
| B、NO2 |
| C、NO |
| D、N2O3 |