题目内容
15.氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得.实验研究认为,该碳热还原反应分两步进行:①Al2O3在碳的还原作用下生成铝的气态低价氧化物X(X中Al与O的质量比为6.75:2);②在碳存在下,X与N2反应生成AlN.请回答:(1)X的化学式为Al2O.
(2)碳热还原制备氮化铝的总反应化学方程式为:
Al2O3(s)+3C(s)+N2(g)?2AlN(s)+3CO(g)
①在温度、容积恒定的反应体系中,CO浓度随时间的变化关系如图曲线甲所示.下列说法不正确的是CD.
A.从a、b两点坐标可求得从a到b时间间隔内该化学反应的平均速率

B.c点切线的斜率表示该化学反应在t时刻的瞬时速率
C.在不同时刻都存在关系:v(N2)=3v(CO)
D.维持温度、容积不变,若减少N2的物质的量进行反应,曲线甲将转变为曲线乙
②一定温度下,在压强为p的反应体系中,平衡时N2的转化率为α,CO的物质的量浓度为c;若温度不变,反应体系的压强减小为0.5p,则N2的平衡转化率将>α (填“<”、“=”或“>”),平衡时CO的物质的量浓度B
A.小于0.5c B.大于0.5c,小于c
C.等于c D.大于c
③该反应只有在高温下才能自发进行,则随着温度升高,反应物Al2O3的平衡转化率将增大(填“增大”、“不变”或“减小”),理由是该反应在高温下自发,且△S>0,所在△H>0,即正反应为吸热反应,升高温度,平衡向正方向移动.
(3)在氮化铝中加入氢氧化钠溶液,加热,吸收产生的氨气,进一步通过酸碱滴定法可以测定氮化铝产品中氮的含量.写出上述过程中氮化铝与氢氧化钠溶液反应的化学方程式AlN+NaOH+H2O=NaAlO2+NH3↑.
分析 (1)依据X中Al与O的质量比为6.75:2计算物质的量之比得到化学式;
(2)①A、图象中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化;
B、c点处的切线的斜率是此时刻物质浓度除以此时刻时间为瞬时速率;
C、化学反应速率之比等于化学方程式计量数之比分析;
D、维持温度、容积不变,若减少N2的物质的量进行反应,平衡逆向进行,达到新的平衡状态;
②若温度不变,反应体系的压强减小为0.5p,平衡向气体体积增大的方向进行,平衡正向进行;
③该反应只有在高温下才能自发进行,结合反应自发进行的判断依据是△H-T△S<0分析;
(3)根据题目信息:AlN溶于强碱溶液时会生成NH3来书写方程式.
解答 解:(1)X中Al与O的质量比为6.75:2计算物质的量之比=$\frac{6.75}{27}$:$\frac{2}{16}$=0.25:0.125=2:1,化学式为:Al2O,
故答案为:Al2O;
(2)①A、图象中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化计算得到,从a、b两点坐标可求得从a到b时间间隔内该化学反应的平均速率,故A正确;
B、c点处的切线的斜率是此时刻物质浓度除以此时刻时间,为一氧化碳的瞬时速率,故B正确;
C、化学反应速率之比等于化学方程式计量数之比分析,3v(N2)=v(CO),故C错误;
D、维持温度、容积不变,若减少N2的物质的量进行反应,平衡逆向进行,达到新的平衡状态,平衡状态与原来的平衡状态不同,故D错误;
故答案为:CD;
②若温度不变,反应体系的压强减小为0.5p,平衡向气体体积增大的方向进行,平衡正向进行,N2的平衡转化率增大,平衡时CO的物质的量浓度增大,CO的物质的量浓度大于0.5c,小于c,故选B,
故答案为:>;B;
③Al2O3(s)+3C(s)+N2(g)?2AlN(s)+3CO(g),反应的熵变大于0,该反应只有在高温下才能自发进行,则△H>0,温度升高平衡正向进行,反应物Al2O3的平衡转化率将增大,
故答案为:增大;该反应在高温下自发,且△S>0,所在△H>0,即正反应为吸热反应,升高温度,平衡向正方向移动;
(3)根据题目信息:AlN溶于强碱溶液时会生成NH3,化学方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑,故答案为:AlN+NaOH+H2O=NaAlO2+NH3↑.
点评 本题考查了化学平衡影响因素分析判断,化学方程式书写方法,主要是图象分析应用,掌握基础是解题关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案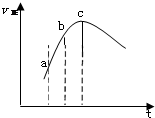 向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应:SO2(g)+NO2(g)?SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如图所示.则正确的结论是( )
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应:SO2(g)+NO2(g)?SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如图所示.则正确的结论是( )| A. | 逆反应速率:a点大于点c | |
| B. | 反应物浓度:a点小于点b | |
| C. | 反应在c点时SO2的转化率最大 | |
| D. | 反应物的总能量低于生成物的总能量 |
| A. | 当生成沉淀达到最大量时,消耗NaOH溶液的体积为150mL | |
| B. | 当金属全部溶解时收集到NO气体的体积为4.48L(标准状况下) | |
| C. | 参加反应的金属的总质量一定是9.9g | |
| D. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.6mol |
| A. | 用电解法制取Na、Mg、Al | |
| B. | 电解熔融NaCl制Cl2 | |
| C. | 以硫或硫铁矿为原料通过接触法制硫酸 | |
| D. | 制硅:SiO2$→_{高温}^{C}$粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$高纯硅 |
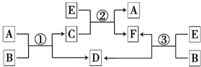 A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物均已给出.
A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物均已给出.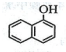 )的同分异构体,其分子中有两个官能团,能发生银镜反应,能被酸性KMnO4溶液氧化成G( C2H4O2)和芳香化合物H(C8H6O4),G和H与碳酸氢钠溶液反应均能放出CO2气体,H芳环上的一硝化产物只有一种.
)的同分异构体,其分子中有两个官能团,能发生银镜反应,能被酸性KMnO4溶液氧化成G( C2H4O2)和芳香化合物H(C8H6O4),G和H与碳酸氢钠溶液反应均能放出CO2气体,H芳环上的一硝化产物只有一种. ;
; +Cu2O↓+2H2O;
+Cu2O↓+2H2O; +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$ +H2O;
+H2O;