题目内容
(13分)摩尔盐[(NH4)2SO4·FeSO4·6H2O]在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂。某研究性学习小组用下图所示的实验装置来制取摩尔盐,实验步骤如下,回答下列问题:
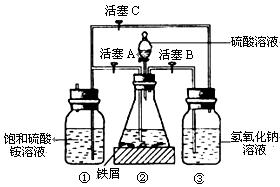
(1) 用30%的NaOH溶液和废铁屑(含少量油污、铁锈等)混合、煮沸,以除去铁屑表面油污,然后冷却、洗涤、分离,将分离出的NaOH溶液装入③中,废铁屑放入②中。
(2) 利用容器②的反应,向容器①中通入氢气,应关闭活塞 ,打开活塞 (填字母)。向容器①中通人氢气的目的是 。
待锥形瓶中的铁屑快反应完时,关闭活塞 ,打开活塞 ②中继续产生的氢气会将 (填①、②或③,后同)容器中的溶液压入① 容器,在常温下放置一段时间,混合溶液底部将结晶析出硫酸亚铁铵。
(3) 为了确定产品中亚铁离子的含量,研究小组用滴定法来测定。
①试配平反应的离子方程式:

②滴定时,将KMnO4溶液装在 (酸式或碱式)滴定管中,判断反应到达滴定终点的现象为 。
(4)装KMnO4滴定管用蒸馏水润洗后,未用KMnO4液润洗导致滴定结果(填“偏小”、“偏大”或“无影响”) 。
(5)观察装KMnO4滴定管读数时,若滴定前仰视,滴定后俯视则结果会导致测得的Fe2+溶液浓度测定值 (选填“偏大”“偏小”或“无影响”)

(1) 用30%的NaOH溶液和废铁屑(含少量油污、铁锈等)混合、煮沸,以除去铁屑表面油污,然后冷却、洗涤、分离,将分离出的NaOH溶液装入③中,废铁屑放入②中。
(2) 利用容器②的反应,向容器①中通入氢气,应关闭活塞 ,打开活塞 (填字母)。向容器①中通人氢气的目的是 。
待锥形瓶中的铁屑快反应完时,关闭活塞 ,打开活塞 ②中继续产生的氢气会将 (填①、②或③,后同)容器中的溶液压入① 容器,在常温下放置一段时间,混合溶液底部将结晶析出硫酸亚铁铵。
(3) 为了确定产品中亚铁离子的含量,研究小组用滴定法来测定。
①试配平反应的离子方程式:

②滴定时,将KMnO4溶液装在 (酸式或碱式)滴定管中,判断反应到达滴定终点的现象为 。
(4)装KMnO4滴定管用蒸馏水润洗后,未用KMnO4液润洗导致滴定结果(填“偏小”、“偏大”或“无影响”) 。
(5)观察装KMnO4滴定管读数时,若滴定前仰视,滴定后俯视则结果会导致测得的Fe2+溶液浓度测定值 (选填“偏大”“偏小”或“无影响”)
(2) A BC 排出饱和硫酸铵溶液及洗气瓶①中的氧气
BC(或B或C)、 A ② ① 各1分,共7分
(3) ① 1 MnO + 5 Fe2++ 8 H+ =" " 1 Mn2++ 5 Fe3++ 4 H2O(2分)
+ 5 Fe2++ 8 H+ =" " 1 Mn2++ 5 Fe3++ 4 H2O(2分)
②酸式,1分 溶液由浅绿色(或无色)变成紫红色,并半分钟内不褪色 2分
(4)偏大(1分)(5)偏小(1分)
BC(或B或C)、 A ② ① 各1分,共7分
(3) ① 1 MnO
 + 5 Fe2++ 8 H+ =" " 1 Mn2++ 5 Fe3++ 4 H2O(2分)
+ 5 Fe2++ 8 H+ =" " 1 Mn2++ 5 Fe3++ 4 H2O(2分)②酸式,1分 溶液由浅绿色(或无色)变成紫红色,并半分钟内不褪色 2分
(4)偏大(1分)(5)偏小(1分)
略

练习册系列答案
相关题目


 器示意图在方框内画出乙烯的发生装置(夹持装置不必画出,需要加热的仪器下方用△标出)。
器示意图在方框内画出乙烯的发生装置(夹持装置不必画出,需要加热的仪器下方用△标出)。 会产生黑烟,实验时若要迅速熄灭火焰,最简单、安全的操作方法是: 。
会产生黑烟,实验时若要迅速熄灭火焰,最简单、安全的操作方法是: 。
 出实验室制乙酸乙酯的化学方程式(要标出氧-18示踪原子)
出实验室制乙酸乙酯的化学方程式(要标出氧-18示踪原子)