题目内容
11.下列有关反应方程式的书写正确的是( )| A. | 泡沫灭火器的灭火原理涉及的离子反应方程式为:Al3++3HCO3-=Al(OH)3↓+3CO2↑ | |
| B. | 将Na2S溶液加入FeCl3溶液中的离子反应方程式为:3S2-+2Fe3++6H2O=2Fe(OH)3↓+3H2S↑ | |
| C. | 已知H2的燃烧热为283 kJ•mol-1,则表示H2燃烧热的热化学方程式为:2 H2 (g)+O2(g)=2 H2O(l)△H=-566 kJ•mol-1 | |
| D. | 向1L 1 mol/L NaOH溶液中加入一定量浓H2SO4溶液至恰好完全反应时,共放出65 kJ的热量.则表示该反应的中和热的热化学方程式为:$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-65kJ•mol-1 |
分析 A.相互促进水解生成大量二氧化碳气体;
B.发生氧化还原反应生成FeS沉淀和S;
C.表示H2燃烧热,氢气的化学计量数为1;
D.浓H2SO4溶液稀释放出大量,则与1molNaOH反应时放出65 kJ的热量,中和热的数值小于65kJ.
解答 解:A.泡沫灭火器的灭火原理为碳酸氢钠与硫酸铝相互促进水解,离子反应方程式为:Al3++3HCO3-=Al(OH)3↓+3CO2↑,故A正确;
B.将Na2S溶液加入FeCl3溶液中的离子反应方程式为3S2-+2Fe3+=2FeS↓+S↓,故B错误;
C.已知H2的燃烧热为283 kJ•mol-1,则表示H2燃烧热的热化学方程式为H2 (g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-283 kJ•mol-1,故C错误;
D.向1L 1 mol/L NaOH溶液中加入一定量浓H2SO4溶液至恰好完全反应时,共放出65 kJ的热量.则表示该反应的中和热的热化学方程式为$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H>-65kJ•mol-1,故D错误;
故选A.
点评 本题考查离子反应及热化学反应方程式书写,为高频考点,把握反应的实质及燃烧热、中和热的判断为解答的关键,侧重分析与应用能力及化学用语的考查,题目难度不大.

练习册系列答案
相关题目
1. 中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者之一.下列说法不正确的是( )
中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者之一.下列说法不正确的是( )
 中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者之一.下列说法不正确的是( )
中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者之一.下列说法不正确的是( )| A. | 从青蒿中提取青蒿素的方法是以萃取原理为基础,萃取是一种化学变化 | |
| B. | 青蒿素的分子式为C15H22O5,它属于有机物 | |
| C. | 人工合成青蒿素经过了长期的实验研究,实验是化学研究的重要手段 | |
| D. | 现代化学分析测试中,可用元素分析仪确定青蒿素中的C、H、O元素 |
2.在核医学中,13153I除了以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病治疗外,还可用来标记许多化合物,供体内或体外诊断疾病用.I-131的中子数是( )
| A. | 131 | B. | 53 | C. | 78 | D. | 184 |
19.下列事实与胶体知识有关的是( )
①用盐卤点豆腐 ②生产出果冻 ③用明矾净水 ④河海交汇处可沉积成沙洲 ⑤初冬凌晨的迷雾的形成.
①用盐卤点豆腐 ②生产出果冻 ③用明矾净水 ④河海交汇处可沉积成沙洲 ⑤初冬凌晨的迷雾的形成.
| A. | 全部都是 | B. | ②③④ | C. | ①③⑤ | D. | ①②③ |
6.能影响水的电离平衡,并使溶液中c(OH -)>c(H+)操作是( )
| A. | 加入NaHCO3晶体 | B. | 加入NaNO3晶体 | ||
| C. | 加入NaHSO4晶体 | D. | 加入NH4Al(SO4)2晶体 |
16.下列关于自发反应的叙述中,正确的是( )
| A. | 凡是放热反应都是自发的,凡是吸热反应都是非自发的 | |
| B. | 自发反应是无需外界条件就能自发进行的化学反应 | |
| C. | 在通常情况下,冰能自行融化,所以它是自发反应 | |
| D. | 由反应CaCO3(s)=CaO(s)+CO2(g)的特点分析可知其在高温下才能自发进行 |
3.下列化学用语的表达正确的是( )
| A. | NaHSO3在溶液中的电离:NaHSO3=Na++H++SO32- | |
| B. | Cl-的结构示意图: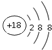 | |
| C. | HClO结构式:H-Cl-O | |
| D. | 医用钡餐的化学式:BaSO4 |
20.对下面①和②两个结构简式的说法中,正确的是( )
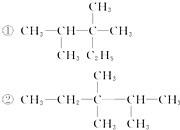

| A. | ①是2,3-二甲基-2-乙基丁烷 ②是3,3,4-三甲基戊烷 | |
| B. | ①②互为同系物 | |
| C. | ①②是同一种物质 | |
| D. | ①②互为同分异构体 |
19.把V L含有MgSO4和Al2(SO4)3的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使铝离子完全转化为AlO2-(1mol铝离子消耗4molNaOH生成1mol AlO2-);另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为BaSO4.则原混合溶液中Mg2+的浓度为( )
| A. | $\frac{8b-3a}{2v}$mol•L-1 | B. | $\frac{8b-3a}{4v}$mol•L-1 | C. | $\frac{8b-3a}{v}$mol•L-1 | D. | $\frac{a-2b}{2v}$mol•L-1 |