题目内容
20.对下面①和②两个结构简式的说法中,正确的是( )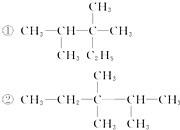
| A. | ①是2,3-二甲基-2-乙基丁烷 ②是3,3,4-三甲基戊烷 | |
| B. | ①②互为同系物 | |
| C. | ①②是同一种物质 | |
| D. | ①②互为同分异构体 |
分析  中两种有机物的主链都是戊烷,在2号C含有1个甲基,在3号C含有2个甲基,二者为同一种物质,其名称为2,3,3-三甲基戊烷,据此进行判断.
中两种有机物的主链都是戊烷,在2号C含有1个甲基,在3号C含有2个甲基,二者为同一种物质,其名称为2,3,3-三甲基戊烷,据此进行判断.
解答 解:①和②两个结构简式相同,属于同一种物质,二者的主链都是戊烷,在2号C含有1个甲基,在3号C含有2个甲基,二者为同一种物质,①和②的名称都为:2,3,3-三甲基戊烷,
故选C.
点评 本题考查了同系物、同分异构体的判断及有机物的命名方法,题目难度不大,明确同系物、同分异构体的概念为解答关键,注意掌握常见有机物的命名方法,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
10.维生素通常根据他们的溶解度来进行分类,它们或者溶解在水中或者溶解在脂肪中.下列维生素中属于水溶性维生素的是( )
| A. | 维生素A | B. | 维生素C族 | C. | 维生素D | D. | 维生素E |
11.下列有关反应方程式的书写正确的是( )
| A. | 泡沫灭火器的灭火原理涉及的离子反应方程式为:Al3++3HCO3-=Al(OH)3↓+3CO2↑ | |
| B. | 将Na2S溶液加入FeCl3溶液中的离子反应方程式为:3S2-+2Fe3++6H2O=2Fe(OH)3↓+3H2S↑ | |
| C. | 已知H2的燃烧热为283 kJ•mol-1,则表示H2燃烧热的热化学方程式为:2 H2 (g)+O2(g)=2 H2O(l)△H=-566 kJ•mol-1 | |
| D. | 向1L 1 mol/L NaOH溶液中加入一定量浓H2SO4溶液至恰好完全反应时,共放出65 kJ的热量.则表示该反应的中和热的热化学方程式为:$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-65kJ•mol-1 |
8.下列实验操作正确的是( )
| A. | 分液时,分液漏斗内上层液体从上口倒出,下层液体从下口倒出 | |
| B. | 过滤时,为加快过滤速度,应用玻璃棒不断搅拌 | |
| C. | 对于互溶的且沸点相差较大的两种液体,可使用蒸馏的方法分离 | |
| D. | 将硫酸铜晶体置于蒸发皿中加热,令其失去结晶水 |
15.下列化合物分子中的所有碳原子不可能处于同一平面的是( )
| A. | 甲苯 | B. | 丙炔 | C. | 丙烯 | D. | 丙烷 |
5.在酸性高锰酸钾溶液中加入过氧化钠粉末,溶液褪色,其中发生反应的离子方程式为:2MnO${\;}_{4}^{-}$+16H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+.下列判断正确的是( )
| A. | O2是还原产物,Mn2+是氧化产物 | |
| B. | Na2O2既是氧化剂,又是还原剂 | |
| C. | 标准状况下,产生22.4L O2时反应转移2mol e- | |
| D. | 通常用浓盐酸酸化高锰酸钾溶液 |
7.700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)反应过程中测定的部分数据见表(表中t1>t2):
依据题意回答下列问题:
(1)反应在t1min内的平均速率为v(H2)=$\frac{0.20}{{t}_{1}}$mol•L-1•min-1
(2)保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2O,到达平衡时,n(CO2)=0.40mol.
(3)保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大(填“增大”或“减小”或“不变”),H2O的体积分数增大(填“增大”或“减小”或“不变”).
(4)温度升至800℃,上述反应平衡常数为0.64,则正反应为放热反应(填“放热”或“吸热”).
(5)700℃时,向容积为2L的密闭容器中充入CO(g)、H2O(g)、CO2(g)、H2(g)的物质的量分别为1.20mol、2.00mol、1.20mol、1.20mol,则平衡向正移动(正、逆、不).
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
(1)反应在t1min内的平均速率为v(H2)=$\frac{0.20}{{t}_{1}}$mol•L-1•min-1
(2)保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2O,到达平衡时,n(CO2)=0.40mol.
(3)保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大(填“增大”或“减小”或“不变”),H2O的体积分数增大(填“增大”或“减小”或“不变”).
(4)温度升至800℃,上述反应平衡常数为0.64,则正反应为放热反应(填“放热”或“吸热”).
(5)700℃时,向容积为2L的密闭容器中充入CO(g)、H2O(g)、CO2(g)、H2(g)的物质的量分别为1.20mol、2.00mol、1.20mol、1.20mol,则平衡向正移动(正、逆、不).