题目内容
14.下列离子方程式正确的是( )| A. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ | |
| B. | 氢氧化钡与稀硫酸混合:SO42-+H++OH-+Ba2+=H2O+BaSO4↓ | |
| C. | 用稀硫酸洗去铁锈:Fe2O3+6H+=2 Fe3++3H2O | |
| D. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓ |
分析 A.根据金属活动顺序表可知:铜不活泼,与稀硫酸不反应;
B.氢氧化钡与硫酸反应生成硫酸钡沉淀和水,硫酸、氢氧化钡电离出的离子不符合其化学式组成;
C.反应生成硫酸铁和水,氧化铁、水在离子反应中保留化学式;
D.石灰乳与Na2CO3溶液反应生成碳酸钙和NaOH,石灰乳在离子反应中应保留化学式.
解答 解:A.在金属活动顺序表中,铜排在氢的后面,所以铜与稀硫酸不反应,故A错误;
B.氢氧化钡溶液与稀硫酸反应生成硫酸钡和水,反应的离子方程式为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故B错误;
C.铁锈主要成分Fe2O3,用稀硫酸洗去铁锈,离子反应为Fe2O3+6H+=3H2O+2Fe3+,故C正确;
D.石灰乳与Na2CO3溶液反应生成碳酸钙和NaOH,石灰乳在离子反应中应保留化学式,离子反应为Ca(OH)2+CO32-═CaCO3↓+2OH-,故D错误;
故选C.
点评 本题考查离子方程式的正误判断,题目难度不大,注意从化学式、离子符号、电荷守恒以及是否符合反应实际的角度分析离子方程式的书写是否正确.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
10.将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是( )
| A. | 参加反应的硝酸的物质的量为0.4mol | |
| B. | 加入合金的质量可能为9.6g | |
| C. | 沉淀完全时消耗NaOH溶液体积为150mL | |
| D. | 溶解合金时产生NO气体体积0.224L(以标准状况) |
9.一定温度下,将 2mol SO2 和 1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g);△H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是( )
| A. | 生成SO3为2 mol | |
| B. | 反应放出197 kJ 的热量 | |
| C. | SO2和SO3物质的量之和一定为2mol | |
| D. | SO2的物质的量和SO3物质的量一定相等 |
6.以下实验能获得成功的是( )
| A. | 检验卤代烃中是否含有氯,可将其与NaOH溶液共热后滴加AgNO3溶液即可 | |
| B. | 根据外加电源的阴极保护法,把钢闸门与外加电源的正极连接就可以被保护 | |
| C. | 将电石与水直接混合可以平稳快速制备乙炔 | |
| D. | CCl4加入盛碘水的分液漏斗中振荡、静置,从下口放出紫红色溶液 |
3.某化学反应2A?B+D在四种不同条件下进行,B、D起始浓度为见反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为0.013mol/(L•min).
(2)在实验2,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是催化剂.
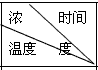 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C1 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C2 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 800℃ | 1.0 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
(1)在实验1,反应在10至20分钟时间内平均速率为0.013mol/(L•min).
(2)在实验2,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是催化剂.
4.短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法正确的是( )
| A. | W、Z、Y、X的原子半径依次减小 | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的弱 | |
| D. | Y的气态简单氢化物的热稳定性比W的强 |