题目内容
下列变化过程,属于放热过程的是
| A.液态水变成水蒸气 | B.酸碱中和反应 |
| C.弱酸电离 | D.NH4Cl晶体与Ba(OH)2·8H2O混合搅拌 |
B
解析试题分析:A.液态水变成水蒸气,是物理变化中的汽化,是吸热过程,故A错误;B.酸碱中和反应,是典型的放热反应,是放热过程,故B正确;C.弱酸电离,是化学变化中的吸热反应,是吸热过程,故C错误;D.NH4Cl晶体与Ba(OH)2?8H2O混合搅拌,是典型的吸热反应,是吸热过程,故D错误;
考点:吸热反应和放热反应

练习册系列答案
相关题目
下列有关能量转换的说法正确的是
| A.煤燃烧是化学能全部转化为热能的过程 |
| B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 |
| C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 |
| D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 |
在25 ℃、101 kPa下,1 g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68 kJ,下列表示甲醇燃烧热的热化学反应方程式是
A.CH3OH(l) +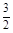 O2(g)=CO2(g)+2H2O(l)△H=+725.8 kJ·mol-1 O2(g)=CO2(g)+2H2O(l)△H=+725.8 kJ·mol-1 |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452 kJ·mol-1 |
C.CH3OH(l) +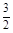 O2(g)=CO2+2H2O△H=-725.8 kJ·mol-1 O2(g)=CO2+2H2O△H=-725.8 kJ·mol-1 |
D.CH3OH(l) +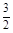 O2(g)=CO2(g)+2H2O(l)△H=-725.8 kJ·mol-1 O2(g)=CO2(g)+2H2O(l)△H=-725.8 kJ·mol-1 |
已知在25℃,101kPa下,lgC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是
| A.C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(g) ?H=-48.40kJ/mol |
| B.C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(1) ?H=-5518kJ/mol |
| C.C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(1) ?H=+5518kJ/mol |
| D.C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(1) ?H=-48.40kJ/mol |
下列说法或表示方法正确的是
| A.反应物的总能量低于生成物的总能量时,该反应一定不能发生 |
| B.在10l kPa、25 ℃时,1 g H2完全燃烧生成气态水,放出120.9 kJ的热量,则氢气的燃烧热为241.8 kJ/mol |
C.已知:2SO2 (g) + O2 (g) 2SO3 (g) ;△H =-98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量 2SO3 (g) ;△H =-98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量 |
| D.由石墨比金刚石稳定可知:C(金刚石,s)= C(石墨,s) ;△H<0 |
下列有关化学反应与能量的说法正确的是
| A.酸碱中和是放热反应 |
| B.炭在氧气中燃烧属于吸热反应 |
| C.化学键的形成需吸收能量 |
| D.化学反应过程中,化学能一定转化成热能 |
以下既有反应热又有溶解热且都是吸热的是
| A.浓硫酸与NaOH溶液 | B.KNO3加入水中 |
| C.NH4NO3加入水中 | D.CaO加入水中 |
已知2H2(g)+O2(g)→2H2O(g)+483.6kJ。下列说法或表达正确的是
| A.在相同的条件下,2mol 氢气与 1 mol 氧气的总能量小于2mol 水蒸气的总能量 |
| B.H2(g)+1/2 O2(g)→H2O(1)+Q1;Q1>241.8kJ |
| C.H2(g)+ 1/2O2(g)→H2O(1)+Q2;Q2<241.8kJ |
| D.任何条件下,2L水蒸气分解成2L氢气与1L氧气需吸收483.6kJ热量 |
下列说法中正确的是
| A.化学反应中的能量变化,表现形式除热量外还可以是光能和电能等 |
| B.化学反应中的能量变化不一定服从能量守恒定律 |
| C.在一个确定的化学反应关系中,反应物的总能量与生成物的总能量可能相同 |
| D.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |