题目内容
下列说法或表示方法正确的是
| A.反应物的总能量低于生成物的总能量时,该反应一定不能发生 |
| B.在10l kPa、25 ℃时,1 g H2完全燃烧生成气态水,放出120.9 kJ的热量,则氢气的燃烧热为241.8 kJ/mol |
C.已知:2SO2 (g) + O2 (g) 2SO3 (g) ;△H =-98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量 2SO3 (g) ;△H =-98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量 |
| D.由石墨比金刚石稳定可知:C(金刚石,s)= C(石墨,s) ;△H<0 |
D
解析试题分析:A、反应物的总能量低于生成物的总能量为吸热反应,有可能发生,错误;B、燃烧热为1mol燃料完全燃烧,生成稳定的产物时得反应热,所以生成气态水的反应热不是燃烧热,错误;C、因为SO2与O2的反应为可逆反应,1 mol SO2和0.5 mol O2不可能完全反应,放出的热量要小于49.15kJ;D、石墨比金刚石稳定,说明石墨的能量低于金刚石,所以金刚石转化为石墨为放热反应,△H<0,正确。
考点:本题考查化学反应与热效应、燃烧热。

练习册系列答案
相关题目
人类将在几十年内逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能等太阳能转换形态),届时人们将适应“低碳经济”和“低碳生活”。下列说法不正确的是
| A.煤、石油和天然气都属于碳素燃料 |
| B.发展太阳能经济有助于减缓温室效应 |
| C.太阳能电池可将太阳能直接转化为电能 |
| D.目前研究菠菜蛋白质“发电”不属于太阳能文明 |
分析能量变化示意图,下列选项正确的是
| A.S(s,单斜)+O2(g)=SO2(g)△H ="+297.16" kJ?mol-1 |
| B.S(s,单斜)+O2(g)=SO2(g)△H ="-296.83" kJ?mol-1 |
| C.S(s,正交)+O2(g)=SO2(g)△H ="-296.83" kJ?mol-1 |
| D.单斜硫比正交硫更稳定 |
形成节约能源和保护生态环境的产业结构是人类与自然和谐发展的重要保证,你认为下列行为中有悖于这一保证的是( )
| A.研究采煤、采油新技术,提高产量以满足工业生产的快速发展 |
| B.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料 |
| C.在农村推广使用沼气 |
| D.减少资源消耗、增加资源的重复使用和资源的循环再生 |
下列反应中的能量变化关系符合如图所示的是
| A.盐酸与烧碱反应 |
| B.天然气燃烧 |
| C.三氧化硫与水反应 |
| D.煅烧石灰石 |
下列变化过程,属于放热过程的是
| A.液态水变成水蒸气 | B.酸碱中和反应 |
| C.弱酸电离 | D.NH4Cl晶体与Ba(OH)2·8H2O混合搅拌 |
已知2H2(g)+O2(g) =2H2O(l)△H=—571.6kJ·mol—1,2H2(g)+O2(g)=2H2O(g)△H=—483.6kJ·mol—1。下列说法正确的是
| A.1molH2O(l)变成1mo1H2O(g),吸收88 kJ能量 |
| B.1 molH2O(g)分解成H2(g)和O2 (g),吸收241.8kJ能量 |
| C.2 molH2(g)和1molO2(g)的总能量小于2molH2O(l)的能量 |
| D.可以寻找特殊催化剂使H2O分解,同时放出能量 |
研制和开发不含碳并可工业生产的清洁能源,一直是科学家不懈追求的目标,目前液氨被人们视为一种潜在的清洁燃料。液氨燃烧的化学反应方程式为:4NH3+3O2 2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
| 燃料 | 沸点(℃) | 燃烧热(kJ/mol) | 相对分子质量 | 液态密度(g/cm3) |
| 氢 | -252.6 | 238.40 | 2.02 | 0.07 |
| 氨 | -33.50 | 317.10 | 17.03 | 0.61 |
①以氨和氢为燃料时,可以减缓温室效应
②氨泄漏到空气中比氢气更易发生爆炸
③等质量的氨和氢分别燃烧,氢放出的热量多
④氨的液化比氢容易得多
A.①③ B.②③ C.①④ D.②④
金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石并需要吸收能量。已知12g石墨或金刚石完全燃烧时放出的热量依次为Q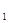 和Q
和Q ,下列说法错误的是
,下列说法错误的是
A.Q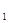 <Q <Q |
| B.石墨不如金刚石稳定 |
| C.质量相等的石墨与金刚石,石墨具有的能量比金刚石低 |
| D.质量相等的石墨与金刚石完全燃烧,生成的二氧化碳一样多 |