题目内容
4.设NA是阿伏加德罗常数的数值,下列说法不正确的是( )| A. | 标准状况下,2.24 L Cl2溶于水,转移的电子数目为0.1NA | |
| B. | 1 mol Na2O和Na2O2混合物中含有的阴、阳离总数是3 NA | |
| C. | 常温常压下,8 g SO3所含的氧原子的数目为0.3NA | |
| D. | 过氧化钠与H2O反应,每生成0.1mol氧气,转移电子的数目为0.2NA |
分析 A.氯气与水反应为可逆反应,不能完全进行到底;
B.过氧化钠中阴离子为过氧根离子,1mol Na2O和Na2O2的混合物中含有的阴、阳离子的物质的量为3mol;
C.根据n=$\frac{m}{M}$计算出 SO3的物质的量,然后根据1mol SO3含3mol氧原子来计算;
D.过氧化钠和水反应方程式为2Na2O2+2H2O=4NaOH+O2↑,每生成1mol氧气转移电子物质的量=1mol×2×[0-(-1)]=2mol,据此计算生成0.1mol氧气转移的电子数.
解答 解:A.标准状况下,2.24L Cl2物质的量为0.1mol,氯气与水反应为可逆反应不能完全进行到底,转移的电子数目小于0.1NA,故A错误;
B.过氧化钠中阴离子为过氧根离子,1mol Na2O和Na2O2的混合物中含有的阴、阳离子的物质的量为3mol,数目为3 NA,故B正确;
C.SO3的物质的量n=$\frac{m}{M}$=$\frac{8g}{80g/mol}$=0.1mol,而1mol SO3含3mol氧原子,故0.1molSO3含0.3mol氧原子,个数为0.3NA,故C正确;
D.过氧化钠与水的反应中,生成0.1mol氧气转移了0.2mol电子,转移电子的数目为0.2NA,故D正确;
故选:A.
点评 本题考查阿伏加德罗常数的相关计算,明确物质的性质、物质结构、物质之间的转化是解题关键,注意过氧化钠中阴离子为过氧根离子.

练习册系列答案
相关题目
14.A、B两容器极易导热,A容器的容积不变,B容器有一个可以上下滑动的活塞,以保持内外压强相等.在相同条件下,将等量的NO2分别压入容积相同的A、B两容器中,反应为:2NO2(g)?N2O4(g)△H<0,下列叙述不正确的是( )
| A. | 反应起始时,两容器中生成N2O4的速率关系是v(A)=v(B) | |
| B. | 反应达到平衡前,两容器中生成N2O4的速率关系是v(A)<v(B) | |
| C. | 反应达到平衡后,NO2的转化率大小关系是v(A)<v(B) | |
| D. | 两容器均达到平衡后,再分别充入等量的氮气,发生平衡移动的是B容器,且平衡移动后,NO2的转化率将增大 |
15. A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
(1)将A、E两种元素的元素符号填入下表中正确的位置上.
(2)A、B、C、D、E、F六种元素中非金属性最强的是F(填元素符号),B、D量元素可以组成原子个数比为1:1的离子化合物,写出该离子化合物的电子式: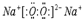 ,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
(3)写出D、F两元素的最高价氧化物对应的水化物反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
 A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.(1)将A、E两种元素的元素符号填入下表中正确的位置上.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | ----------------- | |||||||
| 二 | ||||||||
| 三 | ||||||||
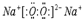 ,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).(3)写出D、F两元素的最高价氧化物对应的水化物反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
12.如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )
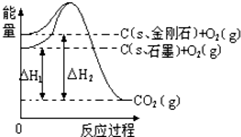

| A. | 石墨和金刚石的转化是物理变化 | |
| B. | 金刚石的稳定性强于石墨 | |
| C. | 1 mol石墨的总键能比1 mol金刚石的总键能大 1.9 kJ | |
| D. | C(s,石墨)=C(s,金刚石),该反应的焓变(△H)为负值 |
19.现代化学键理论认为苯环结构中不存在单双键交替结构,可以作为证据的事实是( )
①苯不能使KMnO4溶液褪色
②苯中碳碳键的键能均相等
③苯能在一定条件下跟H2加成生成环己烷
④经实验测得邻二甲苯仅一种结构
⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不因化学变化而使溴水褪色.
①苯不能使KMnO4溶液褪色
②苯中碳碳键的键能均相等
③苯能在一定条件下跟H2加成生成环己烷
④经实验测得邻二甲苯仅一种结构
⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不因化学变化而使溴水褪色.
| A. | ②③④⑤ | B. | ①③④⑤ | C. | ①②③④ | D. | ①②④⑤ |
16.已知甲、乙、丙三种物质均含有同一种中学常见元素X,其转化关系如下:下列说法不正确的( )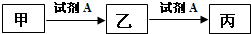
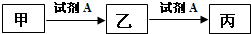
| A. | 若A为硝酸,X为金属元素,则甲与丙反应可生成乙 | |
| B. | 若乙为NaHCO3,则丙一定是CO2 | |
| C. | 若A为金属单质,乙的水溶液遇KSCN溶液变红,则甲可能为非金属单质 | |
| D. | 若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀 |
14.下列关于化学反应与能量的说法正确的是( )
| A. | 中和反应是放热反应 | |
| B. | 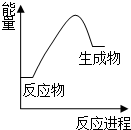 H2燃烧时的能量变化如图所示 | |
| C. | 化学键断裂放出能量 | |
| D. | 反应物总能量与生成物总能量一定相等 |