题目内容
19.标出Zn+H2SO4═ZnSO4+H2↑氧化还原反应的电子转移情况,并指出氧化剂和还原剂.(1)氧化剂是H2SO4;
(2)还原剂是Zn.
(3)电子转移情况如下:
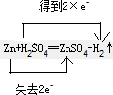 .
.
分析 在反应Zn+H2SO4═ZnSO4+H2↑中,Zn元素的化合价由0升高到+2价,则Zn为还原剂,H元素的化合价由+1降低到0价,则H2SO4为氧化剂,转移电子是2mol;
解答 解:在反应Zn+H2SO4═ZnSO4+H2↑中,Zn元素的化合价由0升高到+2价,则Zn为还原剂,H元素的化合价由+1降低到0价,则H2SO4为氧化剂,
该反应中转移的电子数为2e-,电子转移的方向和数目为 ,故答案为:(1)H2SO4;(2)Zn;
,故答案为:(1)H2SO4;(2)Zn; .
.
点评 本题考查氧化还原反应,为高考常见题型,把握反应中元素的化合价变化为解答的关键,侧重基本概念和转移电子的考查,题目难度不大.

练习册系列答案
相关题目
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,将足量金属镁在2.24LO2中完全燃烧,转移的电子总数为0.2NA | |
| B. | 1L0.1mol.L-1CH3COOH溶液中所含溶质的分子总数小于0.1NA | |
| C. | 将含1molFeCl3的溶液滴入沸水中,所制得的Fe(OH)3胶体粒子为NA | |
| D. | 标准状况下,22.4 L水中含有的氧原子数为1.0NA |
7.“白色污染”的主要危害是( )
①破坏土壤结构 ②降低土壤肥效 ③污染地下水④危及海洋生物的生存.
①破坏土壤结构 ②降低土壤肥效 ③污染地下水④危及海洋生物的生存.
| A. | ①② | B. | ②③ | C. | ①②③④ | D. | ②④ |
14.Ca(OH)2的摩尔质量是( )
| A. | 57g | B. | 57g/mol | C. | 74g | D. | 74g/mol |
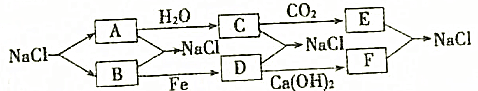
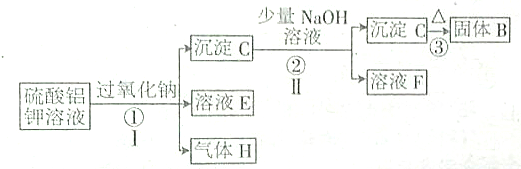
 草酸亚铁可用于合成锂电池的正极材料硅酸亚铁锂(Li2FeSiO4)等,其制备过程主要包括:
草酸亚铁可用于合成锂电池的正极材料硅酸亚铁锂(Li2FeSiO4)等,其制备过程主要包括:
