题目内容
18.下列有关实验操作中合理的是( )| A. | 用托盘天平称取11.70 g食盐 | |
| B. | 用量筒量取12.36 mL盐酸 | |
| C. | 用酸式滴定管量取21.20 mL 0.10 mol•L-1的H2SO4溶液 | |
| D. | 测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,点在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较 |
分析 A.托盘天平的最小读数为0.1g,无法称量到0.01gg的食盐;
B.量筒的最小读数为0.1mL,无法量取到0.01mL盐酸;
C.硫酸为酸性溶液,滴定管能够读到0.01mL;
D.用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.
解答 解:A.托盘天平的最小读数只能读到0.1g,无法用托盘天平称取11.70g食盐,故A错误;
B.量筒的最小读数为0.1mL,无法用量筒量取12.36mL的盐酸,需要使用酸式滴定管量取,故B错误;
C.滴定管能够读到0.01mL的溶液,可以用酸式滴定管量取21.20mL 0.10mol/L H2SO4溶液,故C正确;
D.用水湿润pH试纸,稀释了待测溶液,使呈酸性和碱性溶液的酸碱性减弱,故D错误;
故选C.
点评 本题考查了计量仪器的构造及其使用方法、pH试纸的使用方法,题目难度不大,注意掌握常见的仪器构造及使用方法,明确广泛pH只能读出整数,无法读到小数部分.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.在硫酸铝、硫酸钾和明矾[KAl(SO4)2•12H2O]的混合溶液中,SO42-的浓度为4mol/L,当加入等体积4mol/L KOH溶液时,生成的沉淀恰好完全溶解,则反应后溶液中K+的浓度约为( )
| A. | 9 mol/L | B. | 4.5 mol/L | C. | 2.5 mol/L | D. | 2.25 mol/L |
9.Ⅰ、下表所列物质(括号内为少量杂质),在B中选择试剂,在C中选择操作的方法.填表(填入序号):
B:(1)NaCl细颗粒;(2)NaOH溶液;(3)水;(4)CaO;(5)饱和Na2CO3;(6)溴水;(7)KMnO4溶液.
C:(1)变性;(2)盐析;(3)蒸馏;(4)分液;(5)结晶;(6)洗气.
Ⅱ、1mol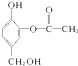 与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
B:(1)NaCl细颗粒;(2)NaOH溶液;(3)水;(4)CaO;(5)饱和Na2CO3;(6)溴水;(7)KMnO4溶液.
C:(1)变性;(2)盐析;(3)蒸馏;(4)分液;(5)结晶;(6)洗气.
| 物质 | 加入试剂 | 操作方法 |
| ①苯(苯甲酸) | (2) | (4) |
| ②乙酸乙酯(乙醇) | (5) | (4) |
 与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
13.下列物质中标*号的原子为sp3杂化的是( )
| A. | $\stackrel{+}{C}$H20 | B. | $\stackrel{+}{N}$H3 | C. | $\stackrel{+}{B}$F3 | D. |  |
3.生活离不开化学,下列物质中不属于餐饮中所涉及的化学物质的是( )
| A. | 乙醇 | B. | 乙酸 | C. | 乙醛 | D. | 乙酸乙酯 |
7.下列粒子在相应的分散系中能大量共存的是( )
| A. | 氢氧化钠溶液:K+、SO32-、CH3COOH、NH3•H2O | |
| B. | 硅酸胶体:H+、K+、SO42-、Br- | |
| C. | 氨水:Na+、Ba2+、Cl-、NO3- | |
| D. | 高锰酸钾溶液:H+、Na+、SO42-、H2O2 |
8.下列说法中正确的是( )
| A. | C60气化和金刚石熔化克服的作用力相同 | |
| B. | 甲酸甲酯的熔点低于乙酸的熔点 | |
| C. | 氯化钠和氯化氢溶于水时,破坏的化学键都是离子键 | |
| D. | 分子晶体的熔沸点低,常温下均呈液态或气态 |

 (2)D和B互为同分异构体,且其苯环上的一氯代物只有两种,D不与NaHCO3反应,能与Na和NaOH反应,等质量的D消耗的Na,NaOH的物质的量之比为2:3,请写出两种D的结构简式为
(2)D和B互为同分异构体,且其苯环上的一氯代物只有两种,D不与NaHCO3反应,能与Na和NaOH反应,等质量的D消耗的Na,NaOH的物质的量之比为2:3,请写出两种D的结构简式为 或
或
 .
.