题目内容
13.常温下,在含CH3COOH和CH3COONa均为0.1mol/L的溶液中,测得pH<7,则下列说法中正确的是( )| A. | c(CH3COO-)<c(Na+) | B. | c(CH3COOH)+c(CH3COO-)=0.2mol/L | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(CH3COO-)>c(Na+) |
分析 物质的量浓度均为0.1mol/L的CH3COOH和CH3COONa混合溶液中,测得pH<7,即c(OH-)<c(H+),由电荷守恒可知c(OH-)+c(CH3COO-)=c(H+)+c(Na+),则测得c(CH3COO-)>c(Na+),即醋酸的电离大于醋酸根离子的水解,并结合物料守恒来解答.
解答 解:A、pH<7,即c(OH-)<c(H+),由电荷守恒可知c(OH-)+c(CH3COO-)=c(H+)+c(Na+),则测得c(CH3COO-)>c(Na+),故A错误;
B、根据物料守恒:c(CH3COOH)+c(CH3COO-)=$\frac{0.1V+0.1V}{V}$=0.2mol/L,故B正确;
C、醋酸的电离大于醋酸根离子的水解,所以c(CH3COOH)<c(CH3COO-),故C错误;
D、pH<7,即c(OH-)<c(H+),由电荷守恒可知c(OH-)+c(CH3COO-)=c(H+)+c(Na+),则测得c(CH3COO-)>c(Na+),故D正确;
故选BD.
点评 本题考查离子浓度大小的比较,明确信息及电荷守恒判断出电离与水解的程度相对大小是解答本题的关键,题目难度中等.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
3.某微粒用${\;}_{Z}^{A}{R}^{n+}$表示,下列关于该微粒的叙述正确的是( )
| A. | 所含质子数=A-n | B. | 所含中子数=A-Z | C. | 所含电子数=Z+n | D. | 质量数=Z+A |
4.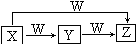 X、Y、Z、W均为中学化学常见物质,一定条件下它们有如图所示的转化关系(某些产物已略去),下列说法错误的是( )
X、Y、Z、W均为中学化学常见物质,一定条件下它们有如图所示的转化关系(某些产物已略去),下列说法错误的是( )
 X、Y、Z、W均为中学化学常见物质,一定条件下它们有如图所示的转化关系(某些产物已略去),下列说法错误的是( )
X、Y、Z、W均为中学化学常见物质,一定条件下它们有如图所示的转化关系(某些产物已略去),下列说法错误的是( )| A. | 若X为HNO3,则W可能为Fe | |
| B. | 若W为O2,X可能是S | |
| C. | 若W为O2,则Z可能为NO | |
| D. | X→Z的离子反应可能为Al3++4OH-=AlO2-+2H2O |
1. 已知A、B、C、D、E、F是周期表中前四周期的六种元素,它们的性质或结构信息如表,请根据信息回答下列问题:
已知A、B、C、D、E、F是周期表中前四周期的六种元素,它们的性质或结构信息如表,请根据信息回答下列问题:
(1)A原子的最外层电子排布式为3s23p4,D原子共有14种不同运动状态的电子,F的离子的价层电子轨道示意图为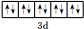 .
.
(2)C与D元素第一电离能的大小关系:Si>Al(填元素符号);
(3)A、B两元素的氢化的分子中键能较小的是H2S(填分子式,下同),分子较稳定的是HCl;
(4)C的单质、镁、NaOH溶液可以构成原电池,则负极的电极反应式为Al-3e-+4OH-=AlO2-+2H2O;
(5)A的氢化物分子中的中心原子的杂化方式为sp3,F的离子可与氨分子形成[F(NH3)4]2+,该阳离子中存在的化学键类型有共价键和配位键;
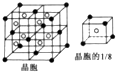
(6)E与钙可组成离子化合物,其晶细胞结构如图所示,该化合物的电子式为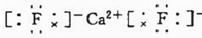 .已知该化合物晶胞$\frac{1}{8}$的体积为2.0×10-23cm3,该离子化合物的密度为3.2g/cm3(保留一位小数).
.已知该化合物晶胞$\frac{1}{8}$的体积为2.0×10-23cm3,该离子化合物的密度为3.2g/cm3(保留一位小数).
 已知A、B、C、D、E、F是周期表中前四周期的六种元素,它们的性质或结构信息如表,请根据信息回答下列问题:
已知A、B、C、D、E、F是周期表中前四周期的六种元素,它们的性质或结构信息如表,请根据信息回答下列问题:| 元素 | 性质或结构信息 |
| A | 单质为黄色粉末,难溶于水,能形成2种二元含氧酸 |
| B | M层有1个未成对的p电子,核外电子总数大于7 |
| C | 与锂形成的合金常用于航天飞行器,单质能溶于强酸和强碱 |
| D | S电子总数比p电子总数少2个,单质或氧化物均具有很高的熔、沸点 |
| E | 周期表中电负性最大的元素 |
| F | 最外层有2个电子,但次外层有18个电子 |
 .
.(2)C与D元素第一电离能的大小关系:Si>Al(填元素符号);
(3)A、B两元素的氢化的分子中键能较小的是H2S(填分子式,下同),分子较稳定的是HCl;
(4)C的单质、镁、NaOH溶液可以构成原电池,则负极的电极反应式为Al-3e-+4OH-=AlO2-+2H2O;
(5)A的氢化物分子中的中心原子的杂化方式为sp3,F的离子可与氨分子形成[F(NH3)4]2+,该阳离子中存在的化学键类型有共价键和配位键;
(6)E与钙可组成离子化合物,其晶细胞结构如图所示,该化合物的电子式为
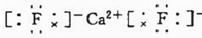 .已知该化合物晶胞$\frac{1}{8}$的体积为2.0×10-23cm3,该离子化合物的密度为3.2g/cm3(保留一位小数).
.已知该化合物晶胞$\frac{1}{8}$的体积为2.0×10-23cm3,该离子化合物的密度为3.2g/cm3(保留一位小数).
8.已知C3N4晶体具有比金刚石还大的硬度,且构成该晶体的微粒间只以单键结合.下列关于C3N4晶体说法错误的是( )
| A. | 该晶体属于原子晶体,其化学键比金刚石更牢固 | |
| B. | 该晶体中每个碳原子连接4个氮原子、每个氮原子连接3个碳原子 | |
| C. | 该晶体中碳原子和氮原子的最外层都满足8电子结构 | |
| D. | 该晶体与金刚石相似,原子间都是非极性键 |
18.下列关于燃料电池的说法正确的是( )
| A. | 燃料电池是通过燃烧方式将化学能转换为电能 | |
| B. | 氢氧燃料电池中,通入氢气的一极为正极 | |
| C. | 氢氧燃料电池是一种环境友好电池 | |
| D. | 燃料电池的能量转化率可达100% |
5.相同质量的锌与酸反应制备H2,欲使反应速率最大,下列条件下的最佳组合是( )
①纯锌片
②粗锌粒
③0.1mol•L-1硫酸
④98%的浓硫酸
⑤加热
⑥用冰水冷却.
①纯锌片
②粗锌粒
③0.1mol•L-1硫酸
④98%的浓硫酸
⑤加热
⑥用冰水冷却.
| A. | ①④⑤ | B. | ②③⑤ | C. | ①③⑥ | D. | ②④⑤ |
2.下列用离子方程式解释正确的是( )
| A. | 用氢氟酸在玻璃上镌刻图案:4I++SiO2═H2O+Si4+ | |
| B. | 向Cu2+、Fe3+混合液中加入CuO除去Fe3+;3H2O+3CuO+2Fe3+═2Fe(OH)3+3Cu2+ | |
| C. | 亚硫酸氢钠溶液显酸性:HSO3-═H++SO32- | |
| D. | 用盐酸与碳酸钠反应证明氯的非金属性强与炭:2H++CO32-═CO2↑+H2O |
14.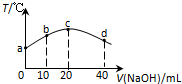 若往20mL 0.01mol•L-l HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )
若往20mL 0.01mol•L-l HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )
 若往20mL 0.01mol•L-l HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )
若往20mL 0.01mol•L-l HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )| A. | HNO2的电离平衡常数:c点>b点 | |
| B. | b点混合溶液显酸性:c(Na+)>c(NO2-)>c(H+)>c(OH-) | |
| C. | c点混合溶液中:c(OH-)>c(HNO2) | |
| D. | d点混合溶液中:c(Na+)>c(OH-)>c(NO2-)>c(H+) |